脊髓损伤动物模型常见模型构建方法、课题设计思路及通路靶点详解!
时间:2025-07-22 阅读:787
常见脊髓损伤动物模型
1. 脊髓打击损伤模型(Contusion)
① 课题研究思路:模拟交通事故/坠落等急性高能量损伤,研究继发性损伤机制(炎症、水肿)、神经保护药物、干细胞移植时机。
② 造模方法:
动物:大鼠(90%文献)、小鼠。
步骤:T10椎板切除 → 暴露脊髓 → 重物(10g砝码)从指定高度(5-25mm)自由落体撞击
成功标志:BMS评分=0分 + 后肢瘫痪 + 尿潴留 + 组织水肿。
③ 优势:损伤程度可量化(高度控制)、临床相关性高、国际通用(NYU、IH打击器标准化)。
④ 局限:需专用设备,出血量影响重复性。
2. 脊髓钳夹损伤模型(Clip Compression)
① 课题研究思路:研究慢性压迫性损伤(椎管狭窄、肿瘤压迫)、减压手术时间窗、微循环障碍机制。
② 造模方法:
动物:大鼠、兔
步骤:T10椎板切除 → 显微镊(压力15-40g)夹持脊髓2-60秒
成功标志:同打击模型 + 组织缺血坏死。
③ 优势:模拟持续压迫病理、操作简单、成本低。
④ 局限:损伤强度依赖操作者经验。
3. 完全横断模型(Complete Transection)
① 课题研究思路:研究轴突再生(神经营养因子、基因治疗)、神经环路重建、电刺激功能恢复。
② 造模方法;
动物:大鼠、斑马鱼(再生研究)
步骤:T9-T10椎板切除 → 显微刀/剪刀完全切断脊髓 → 明胶止血
成功标志:损伤平面下永久性瘫痪 + 组织学确认断端分离。
③ 优势:损伤完全排除自发恢复、再生研究"金标准"。
④ 局限:需长期膀胱护理(人工排尿)、伦理争议大。
4. 球囊压迫模型(Balloon Compression)
① 课题研究思路:模拟慢性压迫(椎间盘突出、椎管狭窄)、渐进性缺血损伤、减压治疗效果评估。
② 造模方法:
动物:兔(血管解剖近人)、猪
步骤:椎板钻孔 → 硬膜外置入球囊导管 → 注入生理盐水(40-50μl)扩张压迫
成功标志:后肢运动障碍 + 影像学确认压迫位置。
③ 优势:损伤可逆(模拟临床减压)、程度可控(注水量调节)。
④ 局限:不适用急性损伤研究。
模型对比
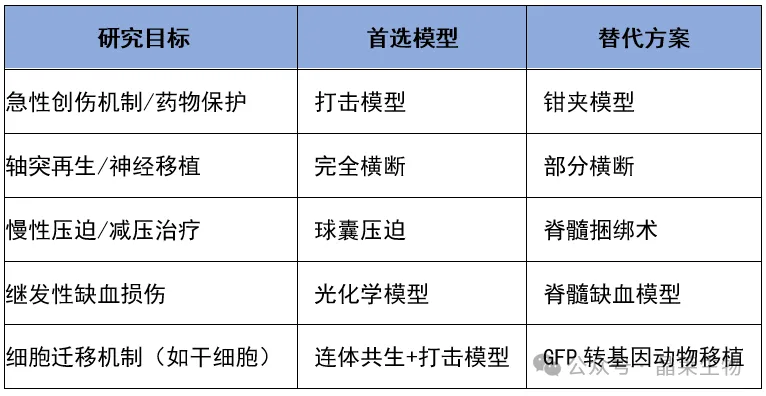
课题设计关键要点
1. 动物选择
① 大鼠:SD/Wistar(通用)、Lewis(免疫耐受移植研究);
② 小鼠:C57BL/6(转基因)、NOD-scid(免疫缺陷移植);
③ 避免使用猫/犬(伦理审查难通过)。
2. 对照组的设置
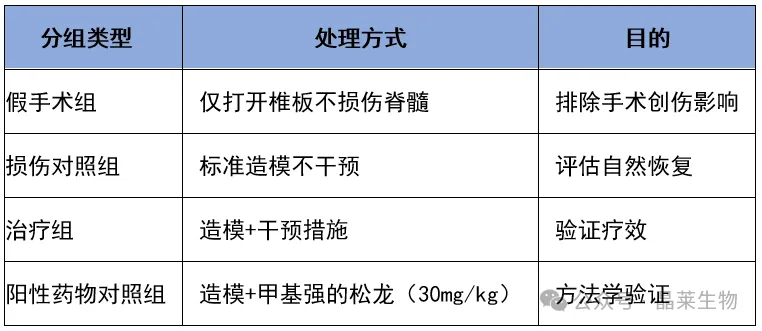
3. 功能评估标准化
① 运动功能:BMS评分(小鼠)、BBB评分(大鼠)
② 感觉功能:热板试验(疼痛阈值)、Von Frey纤毛(触觉过敏)
③ 电生理:运动诱发电位(MEP)、体感诱发电位(SSEP)
④ 影像学:MRI(损伤范围)、Micro-CT(骨性压迫)
4. 组织病理思路
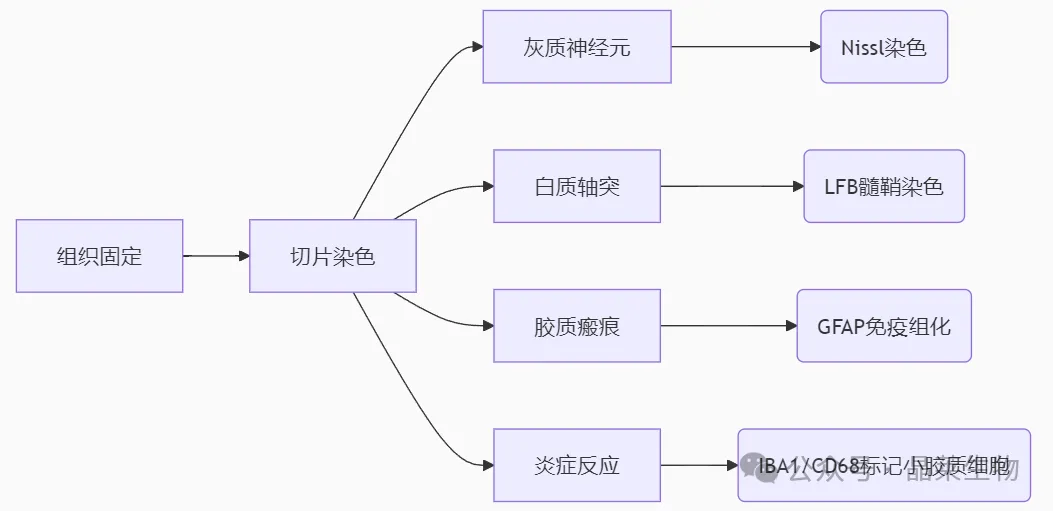
脊髓损伤(SCI)修复研究近年取得显著进展,尤其在分子机制层面揭示了多条关键信号通路。
阐述四种最具转化价值的修复机制:NF-κB炎症调控通路、PI3K/AKT生存信号通路、胶质细胞交互机制及Wnt/PCP神经重塑通路。
1. NF-κB炎症调控通路:Dnm2-OECs的核心修复机制
该通路通过抑制过度炎症反应创造神经再生微环境。最新研究发现,Dynamin-2基因修饰的嗅鞘细胞(Dnm2-OECs)移植后,通过阻断TRAF6/NF-κB信号级联,显著减轻脊髓损伤后的炎症损伤。
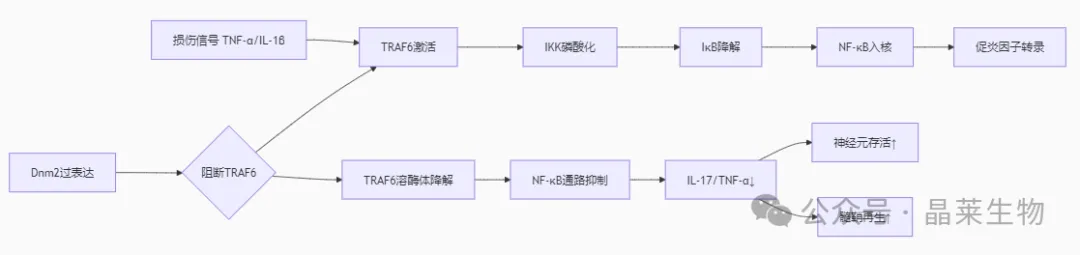
1.1 核心分子事件
上游触发:损伤后小胶质细胞释放的TNF-α、IL-1β等促炎因子激活TRAF6,导致IκB激酶(IKK)复合体磷酸化。
关键调控:Dnm2蛋白直接结合TRAF6,促进其溶酶体降解,阻断IKK-NF-κB通路的激活。
下游效应:NF-κB入核受阻,使IL-17、TNF-α等炎症因子转录减少40%-60%。
表观遗传调控:组蛋白去乙酰化酶(HDAC)活性增强,进一步抑制炎症基因染色质开放度。
1.2 功能效应
神经保护:神经元凋亡率下降50%,线粒体膜电位稳定性提高。
髓鞘再生:髓鞘碱性蛋白(MBP)表达上调2.1倍,G-ratio(轴索/髓鞘直径比)从0.83改善至0.68。
功能恢复:移植28天后大鼠BBB评分从3.2升至12.7,后肢协调性显著改善。
2. PI3K/AKT生存信号通路:双模式神经保护机制
PI3K/AKT通路通过抑制凋亡和氧化应激促进神经存活。研究揭示PD-L1蛋白与淫羊藿活性成分分别通过免疫调节和直接激酶激活两种模式调控该通路。
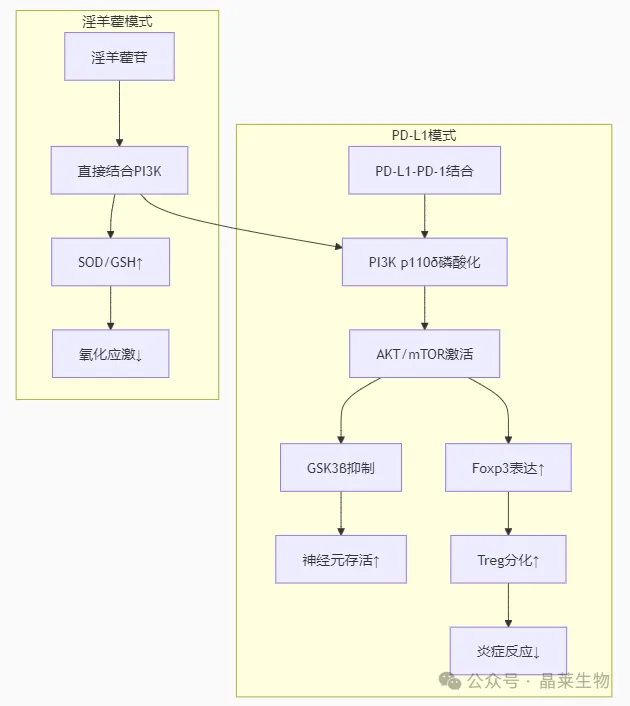
2.1PD-L1的免疫-神经协同机制
配体-受体互作:损伤部位T细胞表达的PD-1与星形胶质细胞PD-L1结合。
通路激活:PI3K p110δ亚基磷酸化,触发AKT(Ser473)/mTORC1级联反应。
免疫调节:促进Th2/Treg分化,抑制Th1/Th17,使IL-10表达升高2.3倍,IFN-γ降低60%。
神经效应:神经元p-GSK3β(Ser9)水平升高,Bax/Bcl-2比率从2.8降至0.9。
2.2 淫羊藿的药理激活机制
活性成分:淫羊藿苷(icariin)穿过血脊髓屏障,直接结合PI3K催化结构域(分子对接得分:-9.3 kcal/mol)。
抗氧化效应:提升SOD/GSH活性150%,降低MDA水平40%
抑制剂验证:LY294002完全阻断淫羊藿介导的AKT激活和运动功能恢复。
功能恢复:治疗组大鼠BBB评分提高78%,空洞面积缩小64%。
3. 胶质细胞交互机制:ET-1/YAP介导的炎症放大
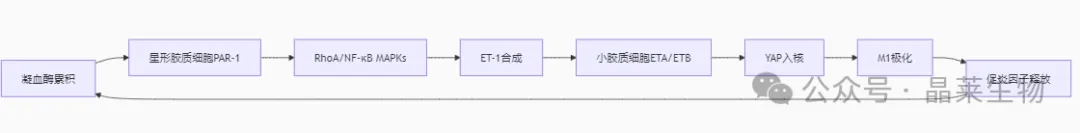
3.1 三阶段信号级联
① 凝血酶感知:血管渗漏导致凝血酶在损伤部位累积(浓度可达2.8 U/mL),星形胶质细胞通过PAR-1受体感知凝血酶信号
② ET-1释放:星形胶质细胞内RhoA/NF-κB和MAPKs双通路激活,启动前内皮素原(prepro-ET-1)转录,释放成熟ET-1
③ 小胶质细胞极化:ET-1与ETA/ETB受体结合,激活小胶质细胞内YAP转录共激活因子,驱动M1型极化标记物表达:
iNOS↑ 3.2倍;CD86↑ 2.7倍;IL-1β分泌量增加4.1倍
3.2 靶向干预策略
PAR-1抑制剂:Vorapaxar(临床抗栓药)使M1细胞比例从68%降至29%
ET受体拮抗剂:波生坦(bosentan)改善运动功能(BBB提高5.3分),效果优于甲基强的松龙。
YAP抑制剂:维替泊芬(verteporfin)阻断下游炎症基因转录。
4. Wnt/PCP神经重塑通路:运动回路可塑性的调节者
非经典Wnt信号通过平面细胞极性(PCP)途径调控轴突再生和突触重塑,其表达与损伤程度密切相关。
4.1 程度依赖性表达调控
轻度损伤(0.45mm):Wnt4/Wnt7a维持基础水平,促进生长锥形成。
重度损伤(0.65mm):
Wnt4↑ 3.1倍:激活RhoA-ROCK,抑制轴突再生。
Wnt7a↓ 60%:减少突触素(synaptophysin)表达,阻碍神经环路重建。
4.2 功能表型关联
运动功能:Wnt4高表达组BMS评分降低42%,步态协调性恶化。
神经病理性疼痛:Wnt7a低表达使机械痛阈值降低55%,与Nav1.3通道表达正相关。
干预策略:Wnt7a重组蛋白局部递送,提高感觉运动整合效率28%。
5. 各通路特性及转化价值:
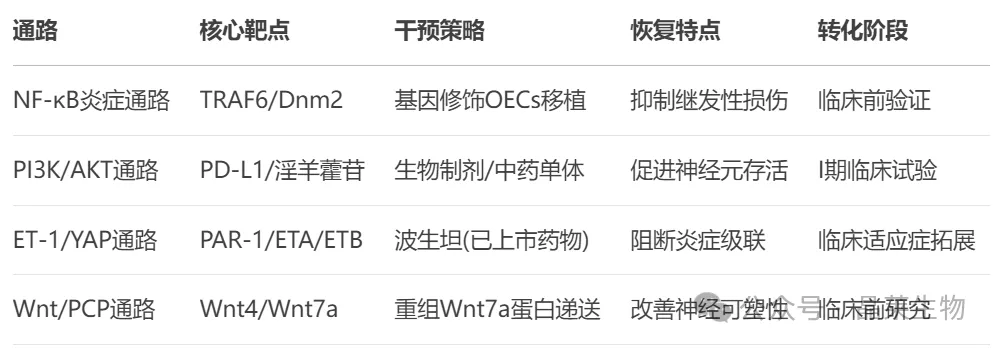
关于晶莱