
时间:2020-12-02浏览次数:6716
世界卫生组织的报告显示称:2022年,全球有230万名妇女被诊断患乳腺癌,有67万人死于乳腺癌。乳腺癌占所有女性癌症的近四分之一,发病比例(46.3%)及死亡比例(13.0%)都高居第一,严重危害着女性的身心健康。
乳腺癌小鼠模型能够模拟人体乳腺癌的发生发展,在疾病发生机理研究,药物新靶点发现及临床前药效学评价等方面具有十分重要的理论价值和临床意义。本期小泷将带大家了解一些常用的乳腺癌模型。
乳腺癌动物模型主要包括移植瘤模型(CDX和PDX模型)、诱导模型(化学、物理和生物学方法)和基因工程模型。
乳腺癌动物模型是研究疾病机制、药物开发和治疗策略的重要工具。不同造模方法模拟乳腺癌的不同分子亚型和病理特征,涉及的关键信号通路和蛋白靶点各有差异。以下是主要模型类型及其机制通路、关键蛋白和临床关联的详细阐述:
一、自发性和化学诱导模型
1. 自发性乳腺癌模型
适用动物:C3H、BALB/c小鼠(MMTV病毒携带者)。
造模机制:小鼠乳腺肿瘤病毒(MMTV)整合到宿主基因组,激活Wnt/β-catenin、Notch等通路,驱动乳腺上皮细胞增殖。
关键蛋白:
Wnt1/β-catenin:维持干细胞特性;
Notch1/4:调控细胞分化和凋亡;
Cyclin D1:促进细胞周期进展。
临床关联:模拟激素受体阳性(HR+)乳腺癌,与人类Luminal亚型相似,用于研究内分泌治疗耐药性。
2. 化学诱导模型
常用试剂:7,12-二甲基苯并蒽(DMBA)、N-甲基亚硝基脲(MNU)。
造模机制:通过DNA烷基化损伤诱导致癌突变,激活雌激素受体(ERα)通路。
关键蛋白:
ERα:介导雌激素依赖性增殖;
Aromatase:促进局部雌激素合成;
CYP1A1/1B1:代谢致癌物生成活性中间体。
临床关联:用于研究ER+乳腺癌的激素治疗(如他莫昔芬)和芳香化酶抑制剂(如来曲唑)。
二、移植模型
1. 同种移植模型(Syngeneic)
方法:将小鼠乳腺癌细胞(如4T1、EMT6)植入免疫健全小鼠。
机制:依赖肿瘤微环境中免疫细胞(TAMs、MDSCs)介导的免疫逃逸。
关键蛋白:
PD-L1:抑制T细胞活性;
CSF-1:招募肿瘤相关巨噬细胞(TAMs);
VEGF:促进血管生成。
临床关联:用于免疫治疗(抗PD-1/PD-L1)和化疗药物(如紫杉醇)的疗效评估。
2. 异种移植模型(Xenograft)
细胞系模型:MDA-MB-231(三阴性)、MCF-7(HR+)、SK-BR-3(HER2+)植入免疫缺陷小鼠(NOD/SCID)。
人源化PDX模型:将患者肿瘤组织直接移植到小鼠,保留原发肿瘤异质性。
关键通路:
HER2/neu(SK-BR-3):激活PI3K/AKT/mTOR和RAS/MAPK通路;
PTEN缺失(MDA-MB-468):导致AKT过度活化。
临床关联:
HER2+模型用于赫赛汀(Trastuzumab)和ADC药物(如T-DM1)的研发;
PDX模型用于个体化治疗筛选。
三、基因工程小鼠模型(GEMMs)
1. 条件性敲除/过表达模型
常见基因:Brca1/2、P53、PIK3CA、PyMT(多瘤病毒中T抗原)。
机制通路:
Brca1/p53双敲除:同源重组修复缺陷,激活PARP依赖性修复;
PyMT驱动:通过Src/Fak通路促进转移。
关键蛋白:
PARP1:DNA损伤修复酶;
E-cadherin:上皮-间质转化(EMT)标志物;
MMP9:促进细胞外基质降解。
临床关联:
BRCA突变模型支持PARP抑制剂(奥拉帕利)的研发;
PI3KCA突变模型验证Alpelisib(PI3K抑制剂)的疗效。
2. 诱导型转基因模型
技术:Tet-On/Tet-Off系统调控基因表达(如HER2、Myc)。
动态研究:可逆性诱导肿瘤生成与消退,模拟疾病进展。
应用:研究癌基因成瘾性(Oncogene Addiction)和靶向治疗耐药机制。
四、原位与转移模型
1. 原位乳腺癌模型
方法:将癌细胞注射到小鼠乳腺脂肪垫(如第四对乳腺)。
优势:模拟肿瘤微环境相互作用,评估局部侵袭和血管生成。
关键蛋白:
HIF-1α:缺氧诱导的转移相关基因;
CXCR4:介导趋化因子导向的转移。
2. 转移模型
常用方法:尾静脉注射(肺转移)、心内注射(骨转移)。
机制:CTC(循环肿瘤细胞)通过整合素-ECM互作定植远端器官。
临床关联:研究转移抑制剂(如Denosumab抗RANKL治疗骨转移)。
五、模型选择与临床转化
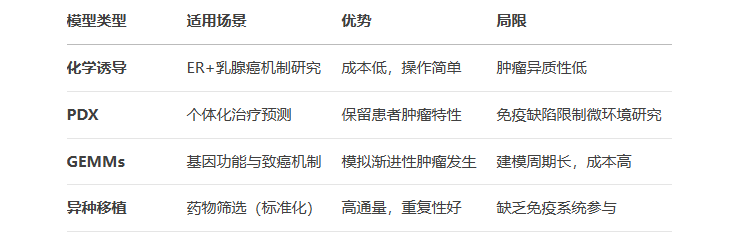
临床研究案例
HER2+模型与赫赛汀:基于HER2转基因小鼠的临床前数据,推动了赫赛汀的III期临床试验(ToGA研究)。
BRCA模型与PARP抑制剂:Brca1缺陷小鼠显示对PARP抑制敏感,支持奥拉帕利获批用于BRCA突变乳腺癌。
免疫治疗验证:4T1模型证明抗CTLA-4联合化疗可增强抗肿瘤免疫,启发临床联合治疗方案设计。
六、未来研究方向
人源化免疫系统模型:将人CD34+干细胞植入NSG小鼠,研究免疫治疗响应。
类器官共培养模型:结合患者来源类器官与免疫细胞,模拟肿瘤-免疫互作。
多组学整合分析:利用单细胞测序和空间转录组技术解析模型与临床样本的分子一致性。
需确认的信息
1. 模型种属(大鼠还是小鼠或是其他种属)
2. 动物体重有无要求,年龄有无要求
3. 雌雄有无要求
4. 模型构建具体方案
5. 取材要求(采血、取组织样本)

上一篇:肺癌动物模型
