
时间:2020-03-16浏览次数:5810
膀胱癌(Bladder cancer,BC)是膀胱黏膜上的恶性肿瘤,是世界上第九大常见恶性肿瘤。其发病率男性比女性高 2~10 倍,死亡率男性为女性 4.0 倍,城市发病率高于农村。有研究者通过实验证实肿瘤微环境对肿瘤进展过程的影响,认为研究膀胱癌发病及转移的机制离不开膀胱癌动物模型。建立理想的膀胱肿瘤动物模型,对于膀胱肿瘤的生物学研究、抗肿瘤药物的研发、人类膀胱癌个体化治疗至关重要。
膀胱肿瘤动物模型主要分为5类:原位致癌物诱发性膀胱癌动物模型、原位移植瘤膀胱癌动物模型、原位自发性膀胱癌动物模型、原位基因工程膀胱癌动物模型、异位膀胱癌动物模型。每一种膀胱癌动物模型都有其优点和缺点,因此实验研究者应按照其实验目的来选择合理的动物模型。
膀胱癌动物模型是研究其发病机制、药物筛选及治疗策略的重要工具。不同造模方法在机制通路、关键蛋白表达及临床转化价值上存在差异。以下从模型构建方法、分子机制通路、关键蛋白及临床研究四方面详细阐述:
一、化学诱导模型(Chemical Carcinogenesis Models)
1. 常用方法
N-甲基亚硝基脲(MNU):膀胱内灌注(剂量5 mg/kg,每周1次,持续6-8周),诱导尿路上皮癌(Urothelial Carcinoma, UC)。
N-丁基-N-(4-羟基丁基)亚硝胺(BBN):0.05% BBN溶于饮用水,持续12-20周,形成侵袭性尿路上皮癌。
MNNG(N-甲基-N'-硝基-N-亚硝基胍):膀胱灌注诱导鳞状细胞癌(SCC)。
2. 机制通路与关键蛋白
HRAS突变:BBN诱导HRAS基因突变,激活MAPK/ERK通路,促进细胞增殖。
EGFR过表达:MNU模型显示EGFR磷酸化增强,激活PI3K/AKT/mTOR通路。
氧化应激:BBN代谢产物损伤DNA,激活Nrf2/KEAP1抗氧化通路,伴随p53突变(约60%模型)。
免疫逃逸:PD-L1上调,抑制CD8+ T细胞功能。
3. 临床研究关联
化疗药物测试:如吉西他滨联合顺铂的疗效验证(与临床II期试验结果一致)。
免疫治疗:抗PD-1抗体在BBN模型中的疗效预测(如KEYNOTE-045试验)。
二、异种移植模型(Xenograft Models)
1. 细胞系来源模型(CDX)
常用细胞系:T24(HRAS突变)、5637(FGFR3突变)、J82(p53缺失)。
构建方法:皮下或膀胱原位注射(5×10^6细胞/小鼠),4-6周成瘤。
2. 患者来源异种移植模型(PDX)
操作:将患者肿瘤组织植入免疫缺陷小鼠(NSG或NOG品系),保留原发肿瘤异质性。
优势:维持肿瘤微环境(TME)及分子亚型(如luminal/basal型)。
3. 机制通路与关键蛋白
FGFR3信号:5637细胞中FGFR3-TACC3融合驱动MAPK通路激活。
细胞周期调控:T24细胞中CDKN2A缺失导致Rb通路失调。
EMT过程:PDX模型中Snail、Vimentin上调,E-cadherin下调。
4. 临床研究关联
靶向治疗:厄达替尼(FGFR3抑制剂)在PDX模型中的响应率与临床试验(BLC2001)相符。
生物标志物筛选:PDX模型用于预测PD-L1表达患者的免疫治疗应答。
三、基因工程模型(Genetically Engineered Models, GEM)
1. 常见模型
UPII-SV40T转基因小鼠:尿路上皮特异性表达SV40大T抗原,抑制p53和Rb,形成高级别UC。
条件性敲除模型:如Upk2-Cre; p53^fl/fl; Pten^fl/fl,诱导肌肉浸润性膀胱癌(MIBC)。
2. 机制通路与关键蛋白
p53/Rb通路失活:SV40T抗原结合p53和Rb,导致基因组不稳定。
PI3K/AKT激活:Pten缺失引发AKT磷酸化,促进肿瘤进展。
Wnt/β-catenin通路:APC基因突变导致β-catenin核聚集,驱动基底型肿瘤。
3. 临床研究关联
分子分型研究:模拟luminal(PPARγ+)和basal(KRT5/6+)亚型,指导靶向治疗。
耐药机制:UPII-SV40T模型揭示顺铂耐药与ERCC1过表达相关。
四、原位模型与转移模型
1. 原位移植
方法:膀胱内注射癌细胞(如MB49细胞系),模拟局部侵袭。
关键机制:CXCL12/CXCR4轴介导肿瘤-间质交互作用。
2. 转移模型
尾静脉注射:筛选高转移潜能细胞(如T24M),研究肺/肝转移。
关键蛋白:MMP-9、VEGF促进血管生成,Twist1诱导EMT。
五、模型选择与临床转化对比
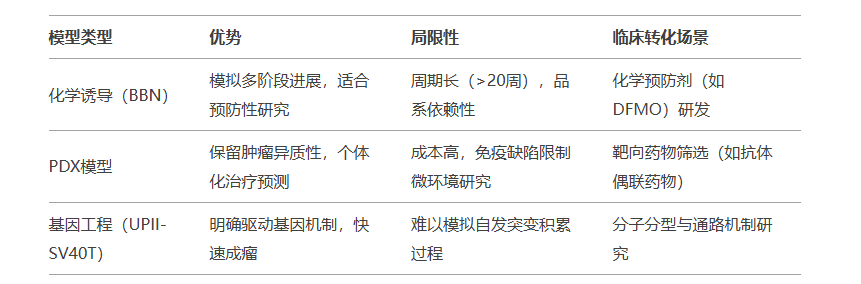
六、未来研究方向
类器官共培养模型:人源膀胱类器官与成纤维细胞/免疫细胞共培养,模拟TME。
CRISPR-Cas9编辑模型:条件性敲除STAG2或KDM6A,研究表观遗传调控。
人源化小鼠模型:重建人免疫系统(如hCD34+ HSPC移植),评估免疫治疗毒性。
通过结合多种模型,可全面解析膀胱癌的分子网络,加速从基础研究到临床应用的转化。
需确认的信息
1. 模型种属(大鼠还是小鼠或是其他种属)
2. 动物体重有无要求,年龄有无要求
3. 雌雄有无要求
4. 模型构建具体方案
5. 取材要求(采血、取组织样本)

上一篇:肾小管间质纤维化动物模型
下一篇:肾结石动物模型
