诺奖热点:核苷修饰mRNA疫苗单次免疫可引起小鼠对SARS-CoV-2的细胞和体液免疫反应
时间:2023-10-16 阅读:1225A Single Immunization with Nucleoside-Modified mRNA Vaccines Elicits Strong Cellular and Humoral Immune Responses against SARS-CoV-2 in Mice
核苷修饰mRNA疫苗单次免疫可引起小鼠对SARS-CoV-2的细胞和体液免疫反应

期刊:Immunity
IF:32.4
接收日期:2020.7.30
研究背景
SARS-CoV-2是COVID-19的病原体,在全球范围内造成了显著的死亡率和发病率,该病毒的迅速传播造成了重大的卫生保健负担以及经济危机,严重威胁了人们的生命安全。
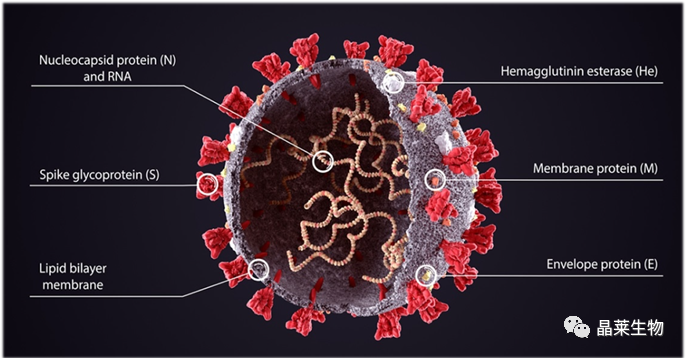
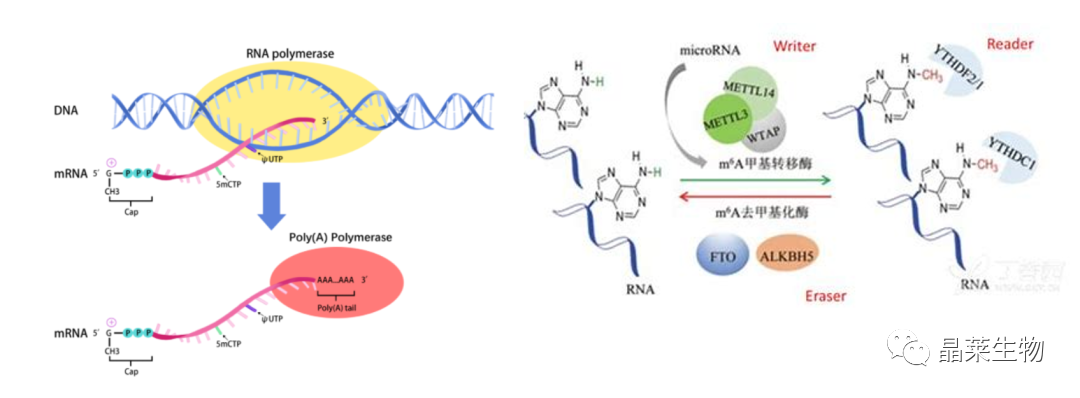
核苷酸碱基修饰是指通过化学或酶学方式对核苷酸上的碱基进行修改或修饰,从而改变核酸的功能或生物学活性。常见的核苷碱基修饰包括甲基化、乙酰化、磷酸化、硫酸化等 。
文献框架&技术路线

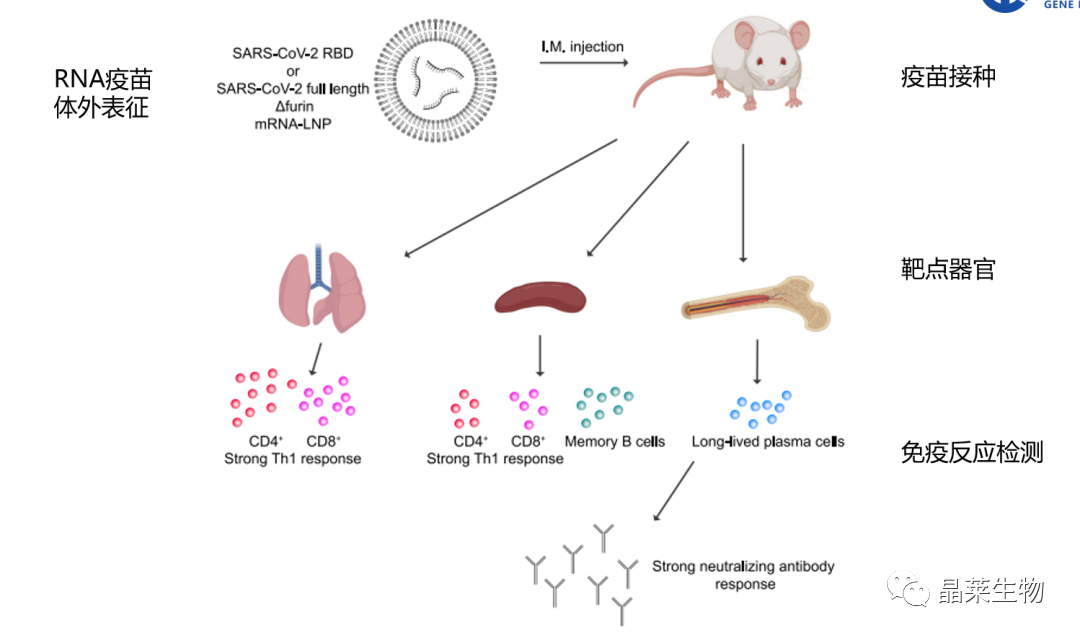
文献框架&技术路线
1. SARS-CoV-2核苷碱基修饰mRNA构建体的体外表征
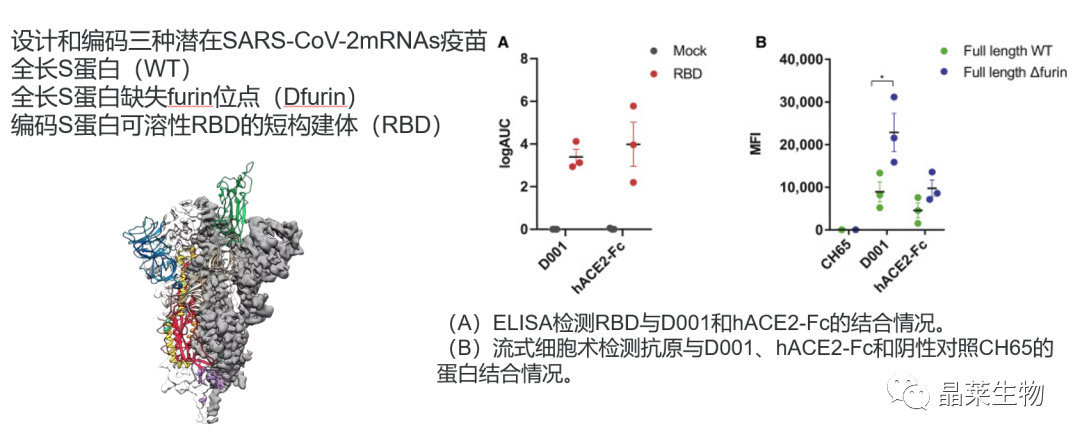
与WT相比,Dfurin对D001和hACE2-Fc具有更高的结合能力,这表明它可能是一种更好的疫苗抗原。
2. SARS-CoV-2 mRNA疫苗诱导S蛋白特异性1型细胞反应
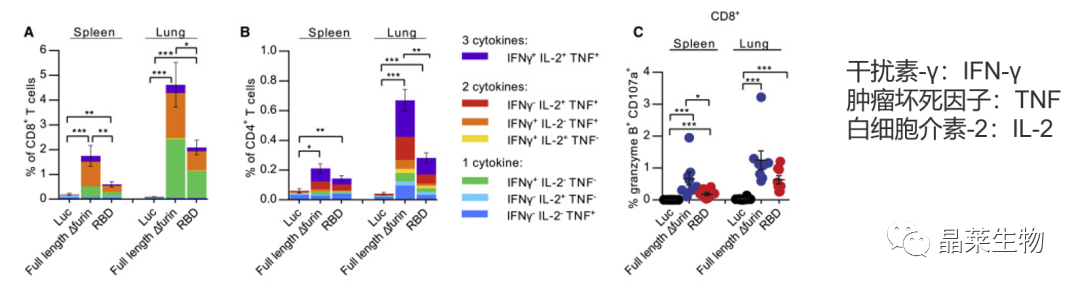
收集免疫后的第10天的小鼠脾脏和肺组织,用SARS-CoV-2 S蛋白多肽池进行刺激,流式细胞术检测CD8+ T细胞(A)和CD4+ T细胞(B)中细胞免疫反应因子的表达,并检测CD8+ T细胞内的细胞毒性标志物。
结果表明SARS-CoV-2 mRNA疫苗可诱导S蛋白特异性1型细胞应答。
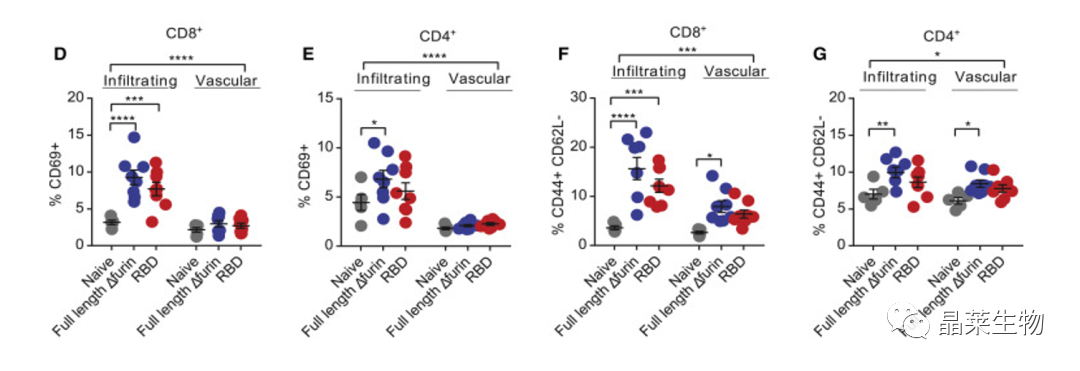
小鼠接种Dfurin、RBD疫苗后,通过细胞标记技术显示肺中T细胞中 CD69+(D、E)和CD44+ CD62L(F、G) 等标志物在组织(i.v.标记阴性)和血管(i.v.标记阳性)的比例。
表明RNA疫苗诱导的T细胞易离开静脉血管系统进入肺实质,同时Dfurin疫苗诱导的T细胞反应比RBD疫苗诱导的更强。
3. SARS-CoV-2 mRNA疫苗能激发有效的和持久的体液免疫反应
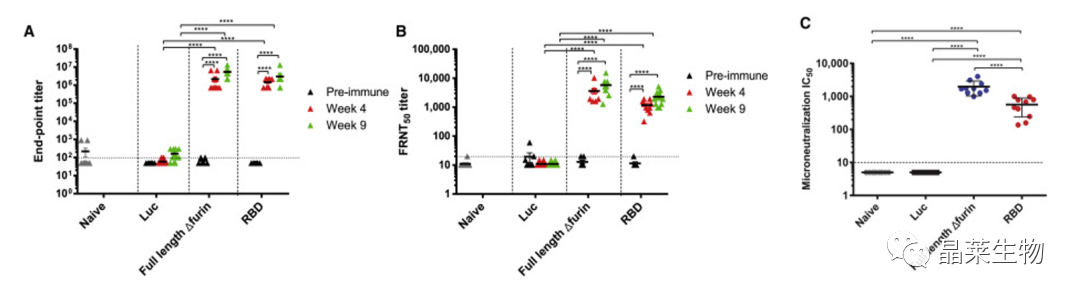
(A)ELISA 检测S蛋白特异性抗体(IgG)水平 (B-C)病毒中和试验检测血清中中和抗体(Nab)水平。
SARS-CoV-2 mRNA疫苗能激发有效和持久的免疫反应,在接种疫苗9周后,Dfurin疫苗产生的中和抗体水平略高于RBD抗原。
4. SARS-CoV-2 mRNA疫苗不会引起体外抗体依赖性感染增强
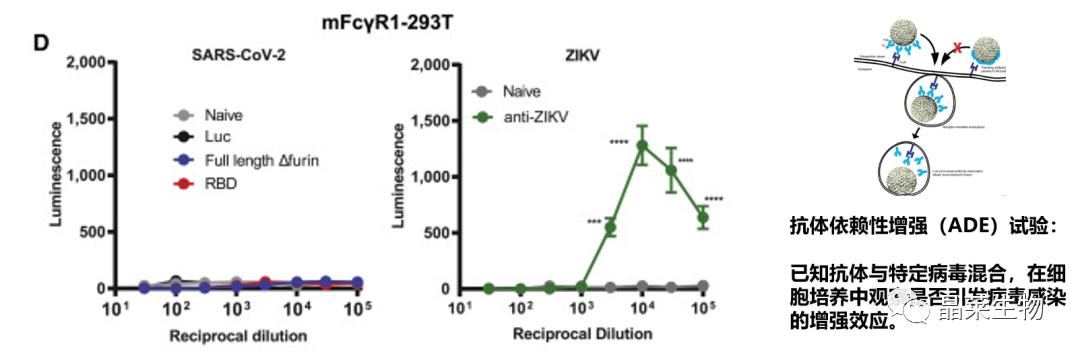
mFcgR1-293T细胞分别感染SARS-CoV-2假病毒和ZIKV病毒颗粒,用免疫9周后抗SARS-CoV-2血清和抗ZIKV血清预孵育。
实验中两种SARS-CoV-2 mRNA疫苗均不会在体外引发抗体依赖性感染增强。
5. SARS-CoV-2 mRNA 疫苗能够诱导强烈的长寿命浆细胞和记忆 B 细胞反应
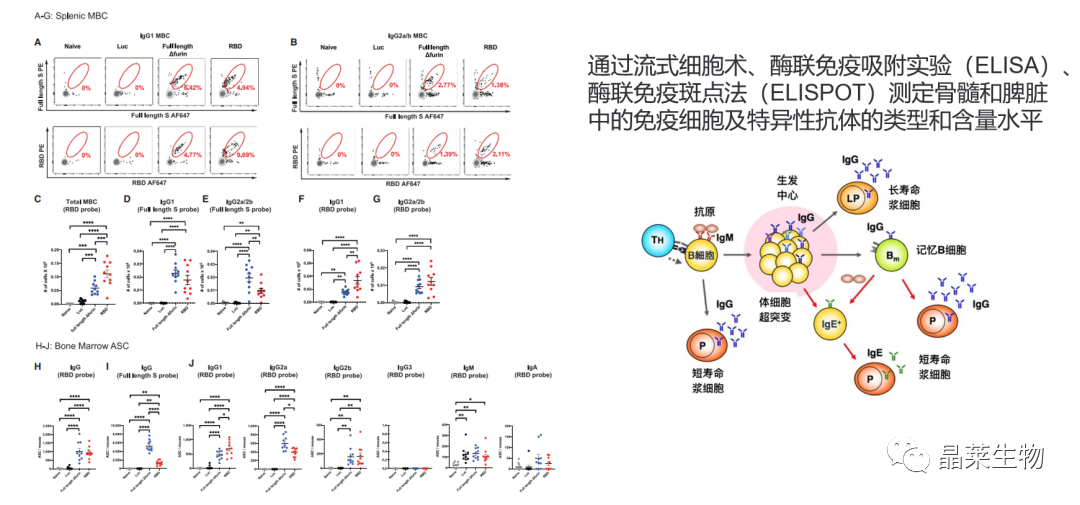
结果表明, SARS-CoV-2 mRNA 疫苗可以在免疫系统中激发两种关键的抗体产生机制,为长期免疫保护提供了支持。
文献结论
核苷修饰mRNA疫苗可诱导较强的T细胞、寿命浆细胞和记忆B细胞等免疫细胞反应,并且有持续的中和抗体反应,同时在体外实验中没有显示抗体依赖性感染增强,是预防和治疗COVID-19的良好候选药物。
文献总结
文献亮点:
1. mRNA疫苗能在脾脏和肺中诱导产生高水平的CD4+和CD8+T细胞反应,诱导产生的T细胞易从血管进入肺中。
2. mRNA疫苗可以诱导显著的记忆B细胞反应,产生具有抗SARS-CoV-2中和活性的抗体。
不足之处:
1. 缺乏评估核苷酸修饰的mRNA-LNP疫苗在动物模型中对SARS-CoV-2的保护效力。
2. 该研究并未设计如何解决疫苗剂量优化问题。此外,小鼠疫苗剂量如何应用于人类免疫,是否与体重成正比、是否受物种间免疫遗传差异影响等问题仍有待于进一步研究。
借鉴意义:
1.基础研究是科技创新的源泉,而好的基础研究往往有其重要临床价值,选择合适的研究方向是基础研究中重要的一部分。
2. mRNA疫苗相较于普通疫苗具有更好的安全性、有效性并能够快速地设计生产, 其相关研究所需的关键技术值得我们进一步的关注与开发。
文献涉及的实验技术
关于晶莱
关注公众号,了解更多!