铁死亡在心血管疾病中的调控机制及相关动物模型构建思路!
时间:2025-05-26 阅读:772
今天小编带大家一起来深入铁死亡与心血管疾病的调控机制及动物模型怎么设计。
1.抑制铁死亡的因素
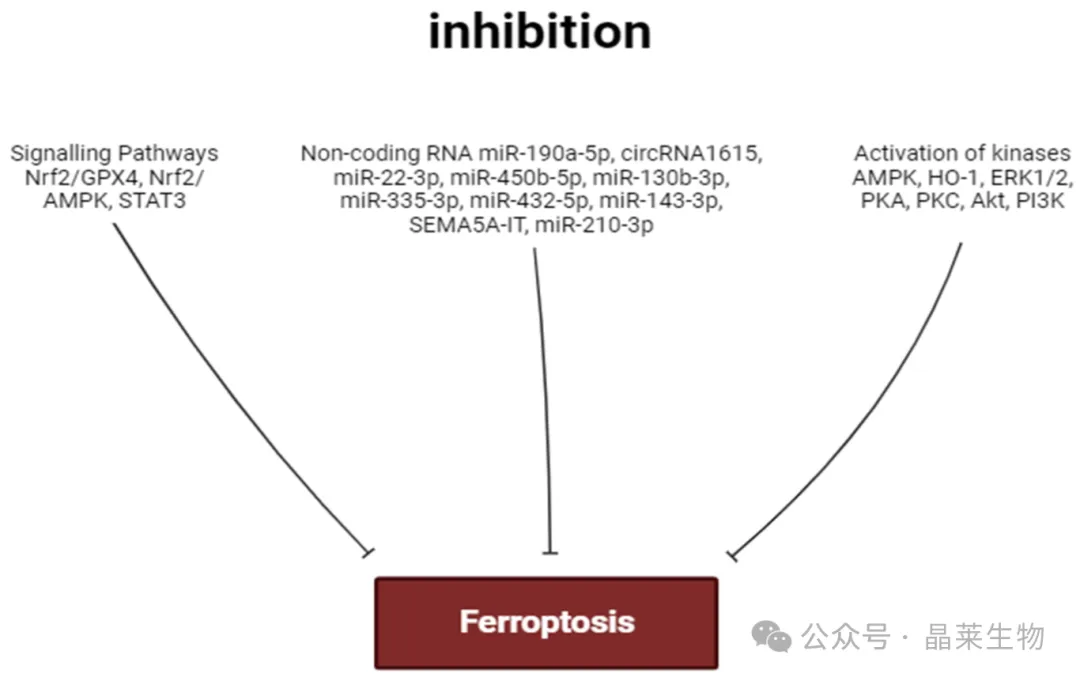
注:垂直箭头是铁死亡的抑制因素。
2.刺激铁死亡的因素

注:箭头是铁死亡的刺激。
3. 铁死亡与心血管疾病
相关研究表明铁死亡与 I/R 心脏损伤、抗肿瘤药物诱导的心肌病、糖尿病心肌病、脓毒性心肌病和炎症的发展有关。有间接证据表明铁死亡参与应激性心脏损伤。
AMPK 、 PKC 、 ERK1/2 、 PI3K 和 Akt 的激活可预防心肌铁死亡。HO-1 的抑制减轻了心肌铁死亡。GSK-3β 和 NOS 在铁死亡调节中的作用需要进一步研究。Nrf2、STAT3 的刺激可防止铁死亡。TLR4 和 NF-κB 的激活促进心肌细胞的铁死亡。
miR-450b-5p 和 miR-210-3p 可以通过抑制铁死亡来增加心肌细胞对缺氧/复氧的耐受性。Circ_0091761 RNA、miR-214-3p、miR-199a-5p、miR-208a/b、miR-375-3p、miR-26b-5p 和 miR-15a-5p 可加重心肌铁死亡。
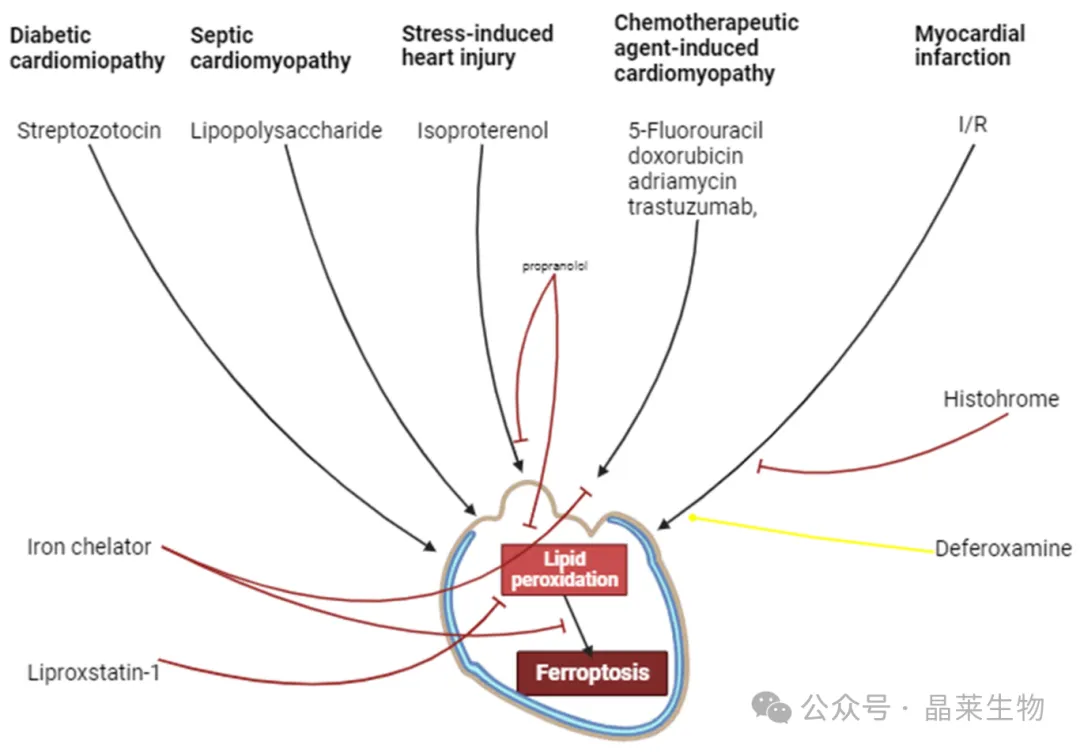
注:黑色箭头是刺激过程,红色和黄色箭头是抑制过程。
4. 铁死亡调节剂在心血管疾病中的应用
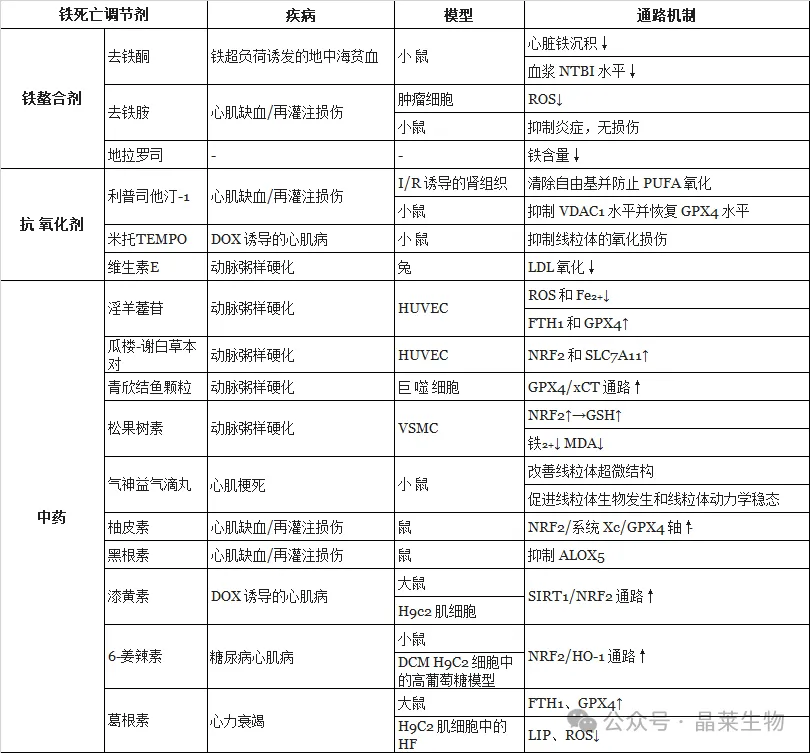
1. 动物选择
① 物种:小鼠(C57BL/6、ApoE⁻/⁻等)或大鼠(SD、Wistar等),根据实验需求选择基因修饰模型(如心脏特异性GPX4敲除小鼠)。
② 年龄与性别:成年动物(8-12周龄),性别需明确(雌雄分笼实验以排除性别差异)。
2. 铁死亡的诱导与干预
① 诱导方法:
药理学诱导:腹腔注射铁死亡诱导剂(如Erastin 10-20 mg/kg,RSL3 5-10 mg/kg,连续3-7天)。
病理模型结合诱导:在心血管疾病模型(如心肌缺血再灌注、动脉粥样硬化)中叠加铁死亡诱导剂或抑制剂。
② 干预策略:
铁死亡抑制剂:Ferrostatin-1(10 mg/kg,腹腔注射)、Liproxstatin-1(5 mg/kg)。
铁螯合剂:去铁胺(DFO,100 mg/kg)或铁调素(Hepcidin)类似物。
3. 评估指标
① 铁代谢相关指标:血清/组织非结合铁(Fe²⁺/Fe³⁺)、铁蛋白(Ferritin)、转铁蛋白受体(TfR1)。
② 脂质过氧化标志物:丙二醛(MDA)、4-羟基壬烯酸(4-HNE)、氧化磷脂(如PEox-AA/AdA)。
③ 组织病理学:心肌/血管组织HE染色、普鲁士蓝染色(铁沉积)、电镜观察线粒体收缩和膜破裂。
④ 功能学检测:心脏超声(EF%、FS%)、血流动力学(左室压力)、心电图(ST段抬高、QT间期)。
⑤ 分子机制验证:检测GPX4、FSP1、ACSL4、SLC7A11(xCT)等关键蛋白表达;Nrf2、HO-1抗氧化通路活性。
4. 对照设计
空白对照组(生理盐水处理)。
疾病模型组(如心肌缺血再灌注)。
疾病模型+铁死亡诱导组。
疾病模型+铁死亡抑制剂组。
1. 心肌缺血再灌注损伤(I/R)
① 模型构建:结扎左冠状动脉前降支(LAD)30分钟,松开后恢复血流(再灌注24-72小时)。
② 铁死亡干预:再灌注期间注射Erastin或RSL3加重损伤,或使用Ferrostatin-1保护心肌。
③ 验证指标:梗死面积(TTC染色)、血清cTnI、CK-MB水平;心肌组织GPX4下调、MDA升高。
2. 动脉粥样硬化(Atherosclerosis)
① 模型构建:ApoE⁻/⁻小鼠高脂饮食(HFD,12周)诱导斑块形成。
② 铁死亡干预:斑块局部注射铁死亡诱导剂(如RSL3)加速斑块不稳定,或使用Liproxstatin-1抑制斑块内脂质过氧化。
③ 验证指标:主动脉油红O染色(斑块面积)、斑块内铁沉积(普鲁士蓝染色)、巨噬细胞焦亡标志物(IL-1β、Caspase-1)。
3. 心力衰竭(Heart Failure)
① 模型构建:主动脉弓缩窄术(TAC)诱导压力超负荷性心衰。
② 铁死亡干预:术后持续给予铁死亡抑制剂(Ferrostatin-1)观察心功能改善。
③ 验证指标:心脏重量/体重比、肺水肿程度、心肌纤维化(Masson染色)、BNP/NT-proBNP表达。
4. 糖尿病心肌病(Diabetic Cardiomyopathy)
① 模型构建:STZ诱导1型糖尿病小鼠(血糖>300 mg/dL持续8周)。
② 铁死亡干预:高糖环境下联合铁死亡诱导剂模拟糖尿病心肌损伤。
③ 验证指标:心肌细胞凋亡(TUNEL染色)、线粒体形态异常(电镜)、ROS生成(DHE荧光染色)。
1. 越来越多的研究表明铁死亡在心血管疾病中的作用和机制,这可能为心血管疾病提供新的治疗和预防策略。
2. 以下问题需要进一步研究:
① 铁蛋白自噬也参与铁死亡,这是否证明铁死亡与其他类型的细胞死亡交叉;
② 铁死亡是脂质过氧化的铁依赖性过程;然而,脂质过氧化导致细胞死亡的具体机制仍不清楚;
③ 铁死亡与心血管疾病(如高血压、心律失常)的关系需要进一步研究;
④ 目前关于铁死亡和心血管疾病的研究大多仍处于细胞和动物实验阶段,未来迫切需要更多的临床研究。
参考文献:
[1]Ferroptosis, a Regulated Form of Cell Death, as a Target for the Development of Novel Drugs Preventing Ischemia/Reperfusion of Cardiac Injury, Cardiomyopathy and Stress-Induced Cardiac Injury by Vyacheslav V. Ryabov,Leonid N. Maslov,Evgeniy V. Vyshlov ,Alexander V. Mukhomedzyanov,Mikhail Kilin,Svetlana V. Gusakova ,Alexandra E. GombozhapovaandOleg O. Panteleev.
[2]Emerging regulatory mechanisms in cardiovascular disease: Ferroptosis Author links open overlay panel Sijie Jin, He Wang, Xiaohao Zhang, Mengyang Song, Bin Liu, Wei Sun
关于晶莱