2024顶刊综述:类器官血管化,看完这篇就够!
时间:2026-05-06 阅读:106
在天然组织中,血管系统承担着营养供应的核心功能,同时调控组织稳态、再生和器官功能。同理,血管化对于类器官培养也至关重要,它能够促进氧气输送、营养转运和代谢废物清除,这些都是维持类器官存活的关键因素。

类器官血管化的必要性与底层生物学核心结论
核心瓶颈定论:哺乳动物组织中氧气与营养物质的扩散极限仅为100~200μm,无功能性血管网络的大尺寸类器官会不可避免地出现核心缺氧、坏死与功能受损,这是限制类器官长期培养、生理复杂度提升与临床转化的最核心障碍。
核心驱动因子定论:血管发生(血管从头形成)与血管生成(现有血管出芽新生)是类器官血管化的两大基础生物学过程,VEGF-A 是该过程最强效、最核心的调控因子;其给药剂量、时空动态直接决定血管网络的分支模式、密度与成熟度,而类器官核心缺氧诱导的内源性 VEGF-A 分泌,是造成类器官批次间差异的关键来源。
非生化调控定论:流体剪切力、细胞外基质(ECM)的理化特性,是血管发育不可替代的非生化调控因素。层流剪切力通过 Piezo1 机械信号通路调控内皮细胞表型与动静脉特化;ECM 的成分、刚度直接决定内皮出芽、血管网络形成与成熟效率,较软的基质更利于微血管网络构建。
微环境交互定论:干细胞微环境与血管网络的双向交互,是维持干细胞干性、谱系分化与血管稳态的核心,复刻该动态交互是实现类器官生理相关血管化的关键前提。类器官可通过血管细胞共培养、血管类器官共培养、类器官共分化、类器官芯片平台和类器官3D生物打印实现血管化。
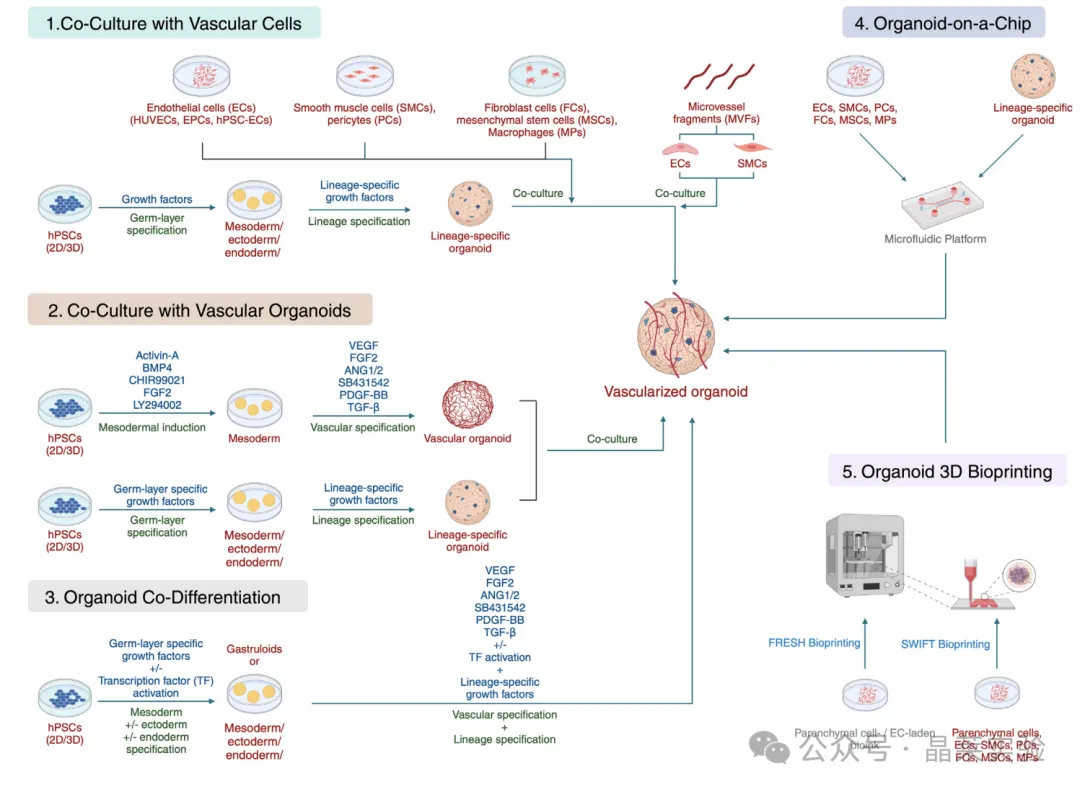
①血管细胞共培养:将内皮细胞(ECs)与支持细胞类型(如周细胞、成纤维细胞)共培养,促进类器官内血管样结构的自组装。
②血管类器官共培养:将谱系特异性类器官与预成型的血管类器官进行策略性共培养,促进二者整合与血管化进程。
③类器官共分化:将干细胞同时分化为器官特异性谱系和血管谱系,实现类器官与其支持血管系统的一体化发育。
④类器官芯片(OOC)技术:将类器官整合到微流控装置中,构建灌注式血管化系统,提升模型的生理相关性。
⑤类器官3D生物打印:通过细胞、生物材料和牺牲墨水的精准沉积,制备具有预设血管通道的类器官,实现对血管结构的更高程度调控。
血管发育由一系列分子因子和信号通路的复杂相互作用所调控,而内皮细胞在适宜的刺激下,具有自组装形成管状结构的内在能力。
这些因子(尤其是VEGF-A)的剂量和给药时机的特异性,在很大程度上决定了类器官内的血管形成模式。
1. VEGF-A的核心作用
结合内皮细胞表面VEGFR1/2,启动血管出芽、尖端细胞竞争、内皮增殖与管腔形成。
与Notch信号协同,决定尖端细胞/茎细胞命运,引导血管向缺氧区延伸。
剂量与时机决定血管网络密度、分支、成熟度,是类器官血管化的关键调控节点。
与FGF-2、Angiopoietin-Tie2、PDGF-β等通路配合,实现血管稳定、周细胞包裹、管腔化。
2. VEGF梯度驱动的血管生成与Piezo1介导的内皮细胞信号传导
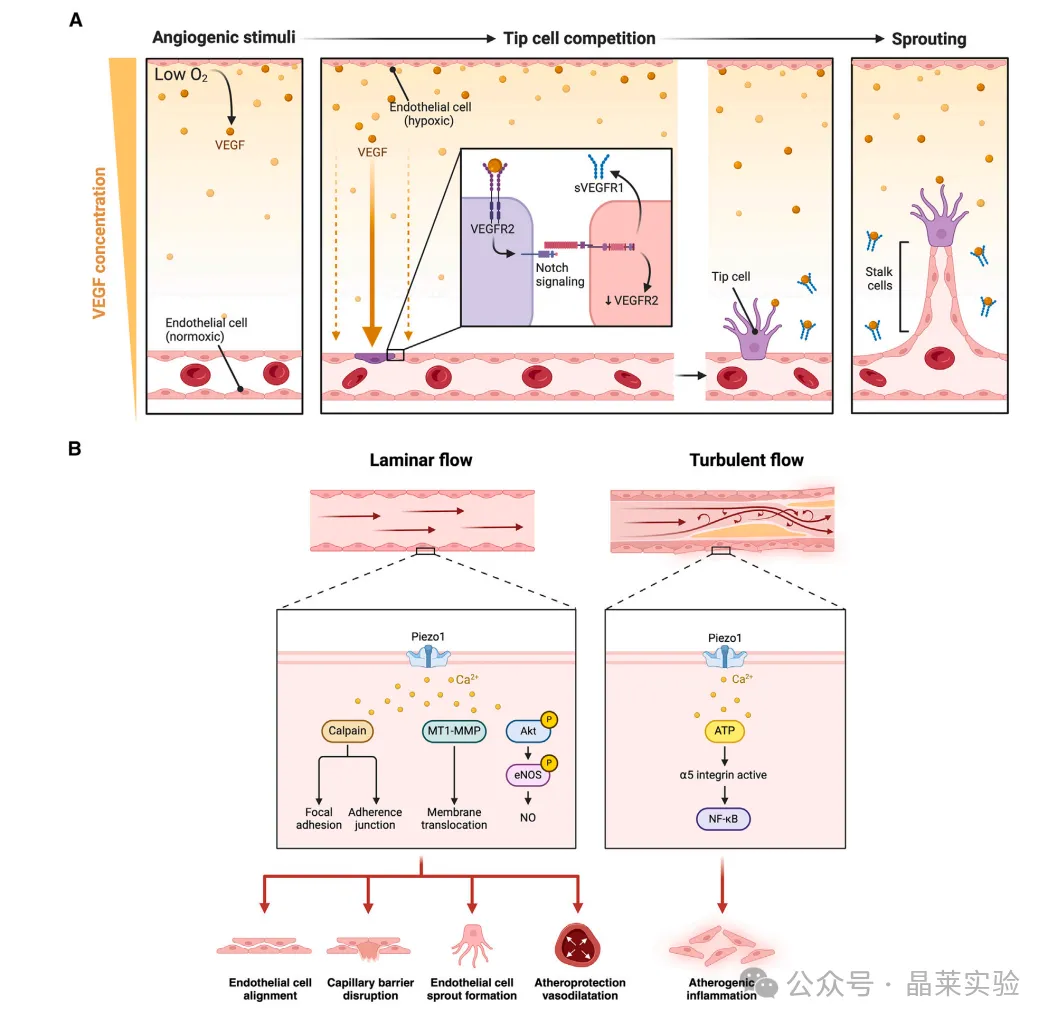
A.缺氧环境下VEGF梯度驱动的血管生成过程。血管生成刺激:血管内壁的内皮细胞暴露于VEGF梯度中,其浓度与组织内的氧分压呈负相关。尖端细胞竞争:响应血管生成梯度,单个细胞高表达VEGFR2,激活邻近细胞的Notch信号。这种细胞间通讯会导致邻近细胞的VEGFR2表达下调、sVEGFR1表达上调,而sVEGFR1可结合并隔离游离的VEGF。相邻尖端细胞之间的这种相互作用,最终决定了哪个细胞成为尖端细胞、哪个细胞保持茎细胞表型。血管出芽:尖端细胞引导血管生成出芽,沿着不断延长的茎细胞向缺氧区域延伸。
B.不同流动条件下Piezo1介导的内皮细胞信号传导。层流条件下(左):Piezo1通道激活引发钙内流,进而启动钙蛋白酶、MT1-MMP、Akt等下游级联反应,使内皮细胞发生一系列生理性改变。湍流条件下(右):Piezo1激活会导致α5整合素活化,长期可促进血管的动脉粥样硬化性炎症反应。
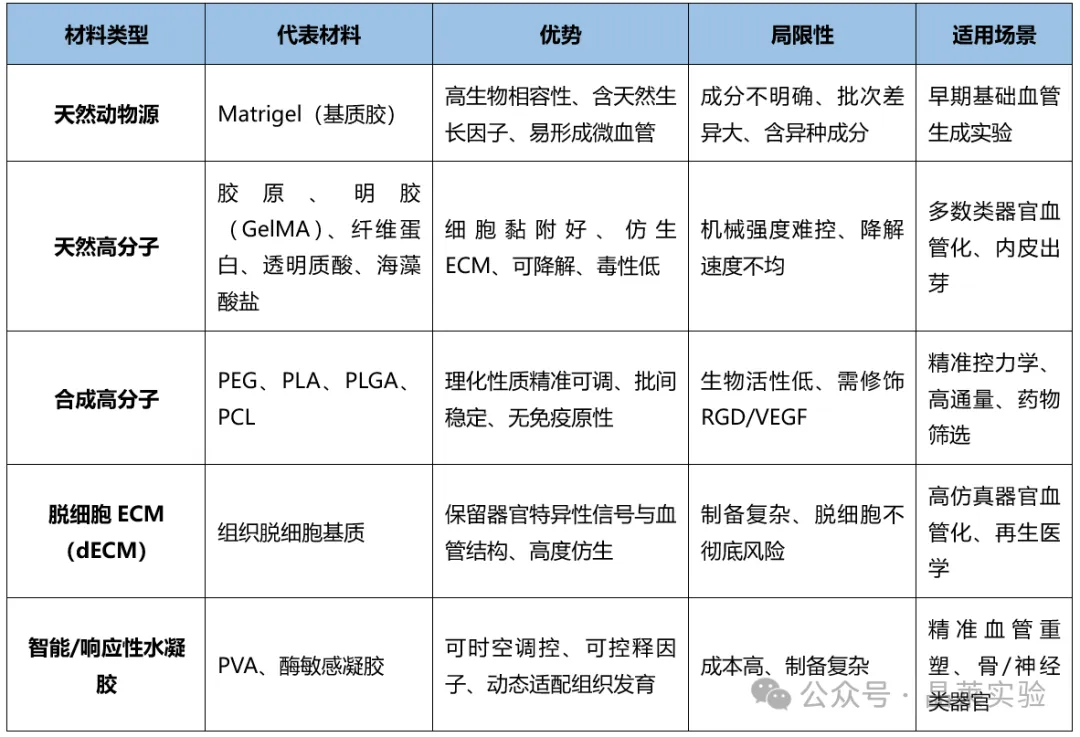
1.各类血管化工程用支架材料
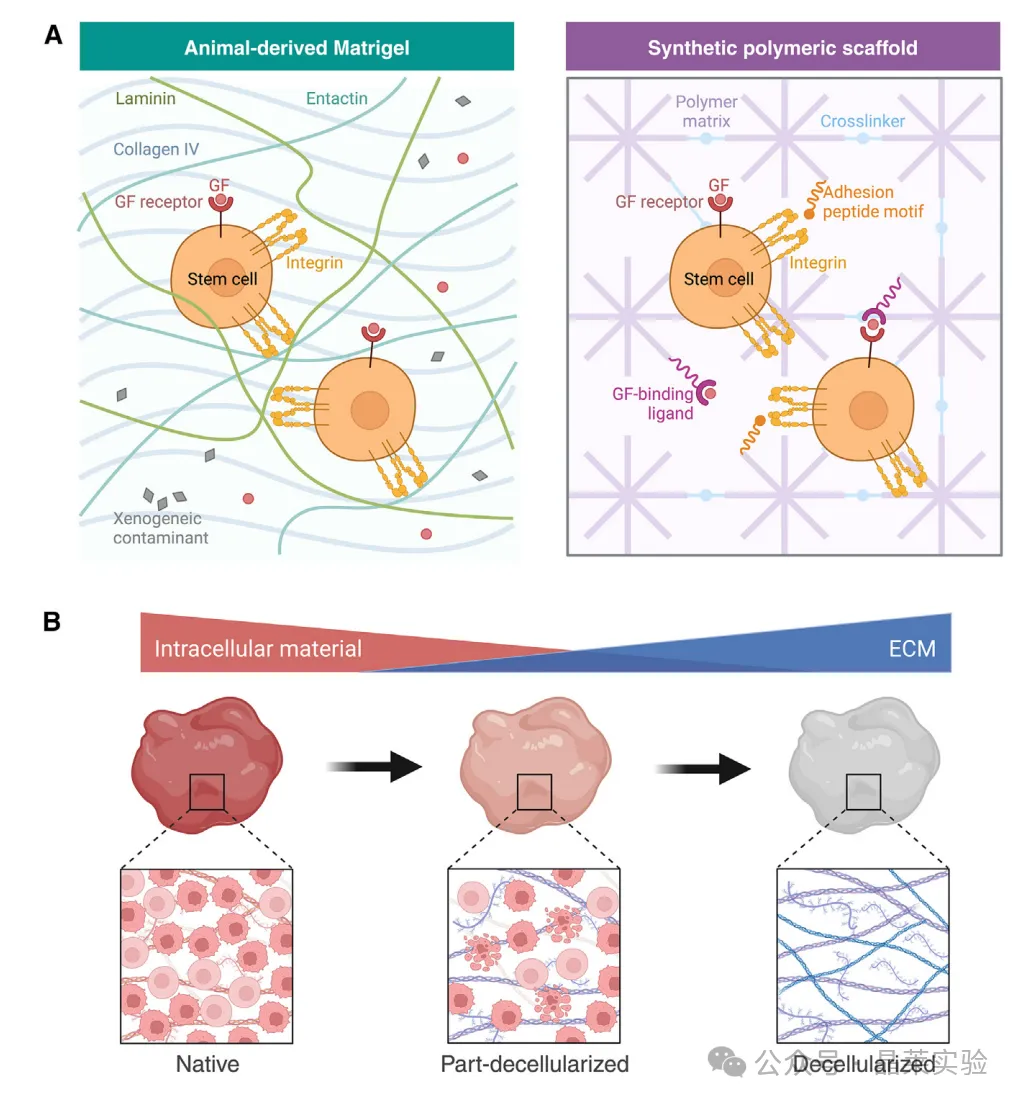
A.类器官工程用动物源支架(左)与合成聚合物支架(右)的对比。动物源基质胶的特点是基质成分复杂、比例不明确,且存在异种污染物和蛋白,可能引发非预期效应和批次间差异;而合成聚合物支架(右)的成分比例明确,理化性质高度可调,能够实现可控的细胞响应。
B.天然组织的脱细胞过程。从左至右展示了从富含细胞成分的天然组织,到细胞内成分减少的部分脱细胞状态,再到富含细胞外基质(ECM)成分的完全脱细胞基质的转变过程,其保留了复杂的细胞外基质架构,可用于类器官血管化。
用于类器官和组织构建体血管化的内皮细胞不同来源对比
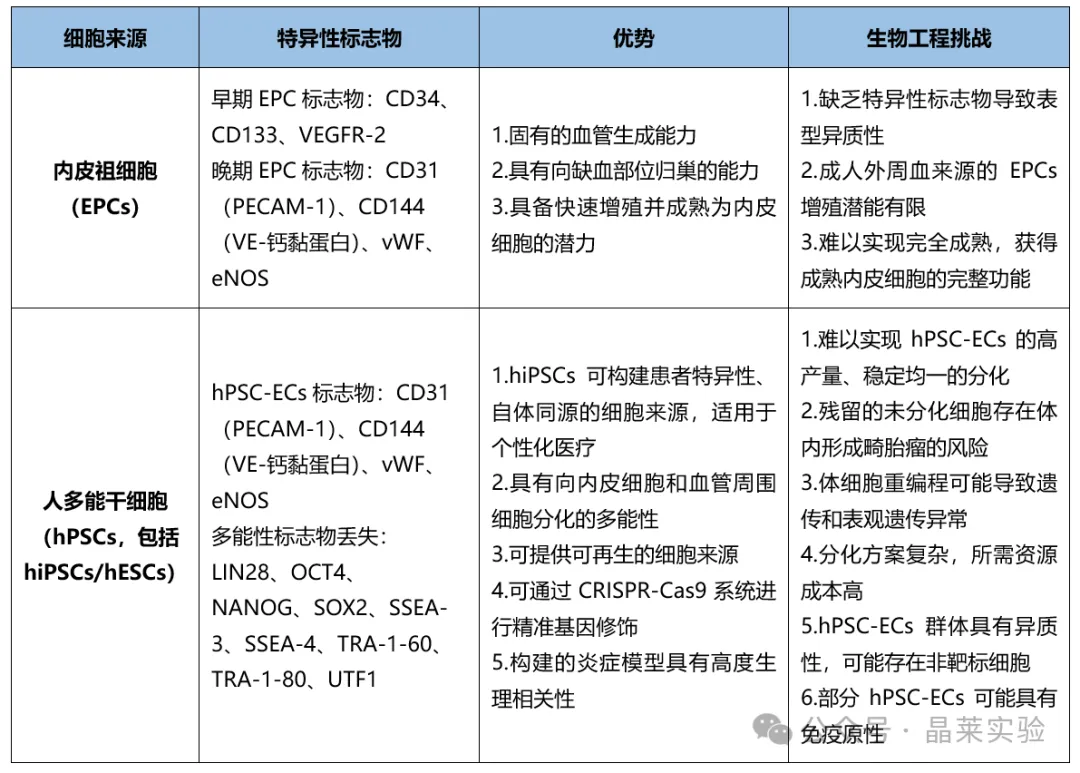
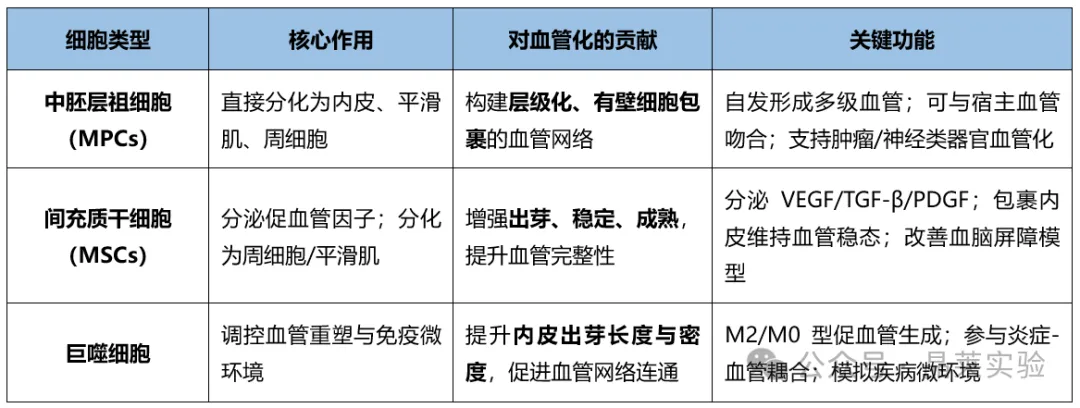
将内皮细胞与经过策略性筛选的支持细胞类型、促血管生成因子(如VEGF、FGF-2)共培养,可驱动细胞自组装形成组织特异性血管结构。近期的研究进展中,通过引入中胚层祖细胞(MPCs)、间充质干细胞(MSCs)和巨噬细胞,进一步提升了类器官模型的血管化效率和血管成熟度:
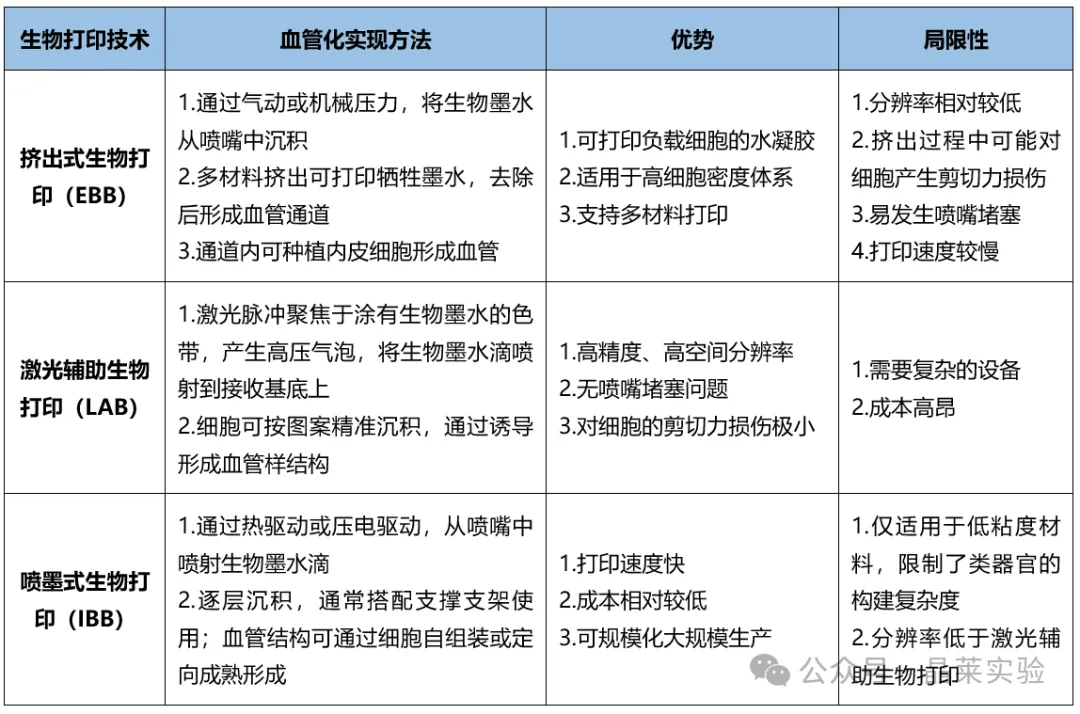
主流类器官3D生物打印技术及其血管化实现方法
血管化类器官已在糖尿病血管病变、早衰症、肿瘤、神经退行性疾病等模型构建,以及药物毒性筛选、个性化药效评价中展现出不可替代的价值,患者特异性 iPSC 来源的血管化类器官,是实现精准医疗的核心工具。
当前血管化类器官向临床与商业化转化存在三大核心瓶颈:一是批次间可重复性差,受细胞来源、培养条件、因子动态的影响显著;二是规模化生产难度大,难以实现高通量、均一化的制备;三是成本高昂,专用设备、生长因子、生物墨水的高成本限制了其广泛应用。
关于晶莱














