Nature Communications|一套纳米颗粒递送两类药物!mRNA 联合 PD-L1 抗体重塑胶质母细胞瘤免疫微环境
时间:2026-05-08 阅读:102
胶质母细胞瘤(glioblastoma,GBM)是侵袭性很强的原发性脑肿瘤。手术、放疗和替莫唑胺化疗仍是主要治疗手段,但肿瘤复发率高,免疫治疗效果也受到多重限制:
血脑屏障(BBB)会限制抗体、核酸等生物制剂的递送;以及高度免疫抑制的肿瘤微环境(TME),其中肿瘤相关巨噬细胞(TAM)是核心调控细胞,占肿瘤内细胞总数的30%–50%。
TAM与肿瘤细胞的直接相互作用会促进肿瘤生长与免疫逃逸,这凸显出亟需研发既能穿透血脑屏障、又能重编程免疫抑制微环境的治疗策略。

2026 年 4 月,东南大学谢金兵、朱旖旎团队在Nature Communications(IF=15.7)发表研究论文 “Co-delivering macrophage engager mRNA and PD-L1 antibody via tumor-responsive nanoparticles for glioblastoma immunotherapy”。
本研究构建了PL@mBiME这一多功能脂质纳米粒(LNP)平台,可实现脑肿瘤靶向递送,并在体内持续表达编码双特异性巨噬细胞衔接器(BiME)的 mRNA。
该 BiME 可同时靶向胶质瘤细胞上的ErbB2与 M2 型巨噬细胞上的CD206,将巨噬细胞重编程为促炎 M1 表型,同时促进巨噬细胞与肿瘤细胞的桥接,增强肿瘤细胞吞噬与抗原呈递。
PL@mBiME整合了pH 响应型电荷反转以提升肿瘤富集与溶酶体逃逸能力,并通过谷胱甘肽触发释放表面偶联的PD-L1 抗体,进一步放大抗肿瘤免疫效应。
在多种胶质母细胞瘤模型中,这种先天免疫与适应性免疫协同激活的策略可诱导肿瘤消退、延长生存期并形成持久的免疫记忆,且无明显毒性。
1. 构建肿瘤响应型 LNP 递送平台 PL@mBiME
研究团队将脑肿瘤靶向递送、mRNA 表达、巨噬细胞衔接器构建和 PD-L1 抗体释放整合到同一纳米颗粒系统中。
2. 利用 mRNA 在体内表达双特异性巨噬细胞衔接器
BiME 同时靶向胶质瘤细胞上的 ErbB2 和 M2 型巨噬细胞上的 CD206,用于促进巨噬细胞与肿瘤细胞的桥接。
3. 推动肿瘤相关巨噬细胞向促炎表型转变
PL@mBiME 处理后,巨噬细胞吞噬肿瘤细胞和抗原呈递相关能力增强,免疫抑制型巨噬细胞被重新拉回抗肿瘤反应中。
4. PD-L1 抗体释放进一步增强 T 细胞免疫反应
该体系通过谷胱甘肽响应方式释放表面偶联的 PD-L1 抗体,配合 BiME 介导的巨噬细胞重编程,形成先天免疫和适应性免疫的联动。
5.在多个 GBM 模型中验证体内疗效
PL@mBiME 在多个 GBM 模型中诱导肿瘤消退,并延长了小鼠生存时间,同时观察到较持久的免疫记忆,未见明显毒性。
1. PL@mBiME 的设计:从 T 细胞衔接转向巨噬细胞衔接
双特异性免疫细胞衔接器的基本思路,是通过一个分子同时识别肿瘤细胞和效应免疫细胞,从而拉近二者距离并增强免疫清除。
以 T 细胞衔接器为代表的策略在部分血液肿瘤中已有较多研究基础,但用于 GBM 等实体瘤时,常会受到 T 细胞浸润不足、药物穿透能力有限以及全身性免疫毒性等因素限制。
研究团队围绕肿瘤内部已有的巨噬细胞作为可调动对象。BiME 的结构围绕这一思路设计:靶向 ErbB2 的抗体片段用于识别胶质瘤细胞,靶向 CD206 的 RP-182 肽用于结合 M2 型巨噬细胞。两端同时发挥作用后,巨噬细胞更容易接近并吞噬肿瘤细胞。
LNP 包载 BiME mRNA,使局部细胞表达巨噬细胞衔接器;酸性环境下的电荷反转有助于提高细胞摄取和内体逃逸;表面偶联的 PD-L1 抗体可在还原性环境中释放,用于解除 T 细胞免疫抑制。通过以上实验设计,研究团队将先天免疫调动和适应性免疫增强放入同一递送体系中。
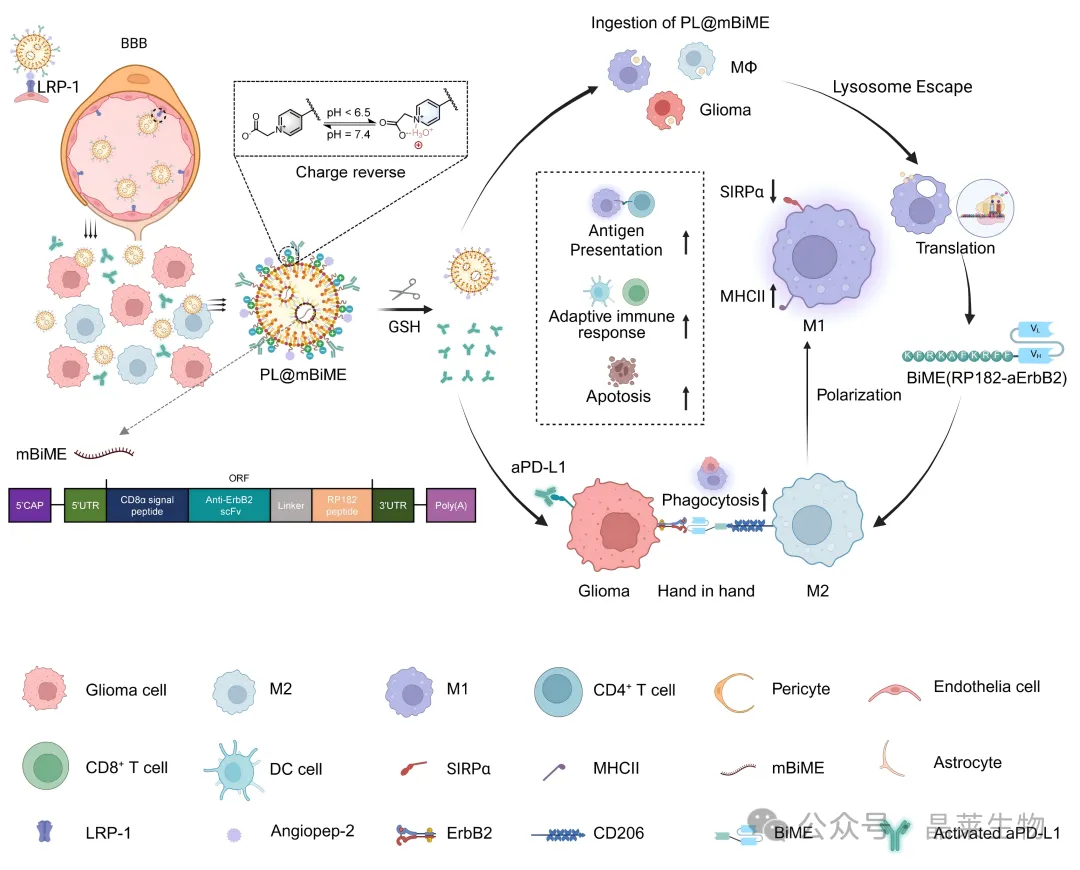
A. PL@mBiME 进入脑肿瘤区域;B. 酸性环境促进颗粒摄取和内体逃逸;C. mRNA 在细胞内表达 BiME;D. BiME 连接 ErbB2⁺ 胶质瘤细胞和 CD206⁺ 巨噬细胞;E. PD-L1 抗体释放后进一步增强 T 细胞抗 肿瘤反应。
2. 纳米颗粒构建与表征:递送系统决定后续免疫调控效率
mRNA 要在体内发挥作用,首先需要在递送过程中保持稳定,并顺利进入细胞、完成胞质释放。研究者由此对 PL@mBiME 的粒径、电位、mRNA 包封能力、形态稳定性以及响应性释放特征进行了系统表征。
从粒径分布和颗粒形态来看,PL@mBiME 形成了相对均一的纳米结构,有利于后续体内循环和组织分布。凝胶阻滞和包封实验结果显示,该体系能够有效包载 mRNA,减少递送过程中的提前降解。
此外,pH响应型电荷反转脂质可在酸性TME中增强摄取。
在正常生理条件下,颗粒表面电荷保持相对稳定;进入偏酸性的肿瘤微环境后,电荷反转增强细胞摄取。对于 mRNA 递送而言,颗粒进入细胞后能否逃离内体,直接关系到目标蛋白表达水平。
PD-L1 抗体则通过二硫键连接在颗粒表面。该连接方式使抗体在循环中相对稳定,并在谷胱甘肽水平较高的肿瘤相关环境中逐步释放。这样可以尽量减少非靶部位提前释放,同时提高肿瘤局部免疫检查点阻断效率。
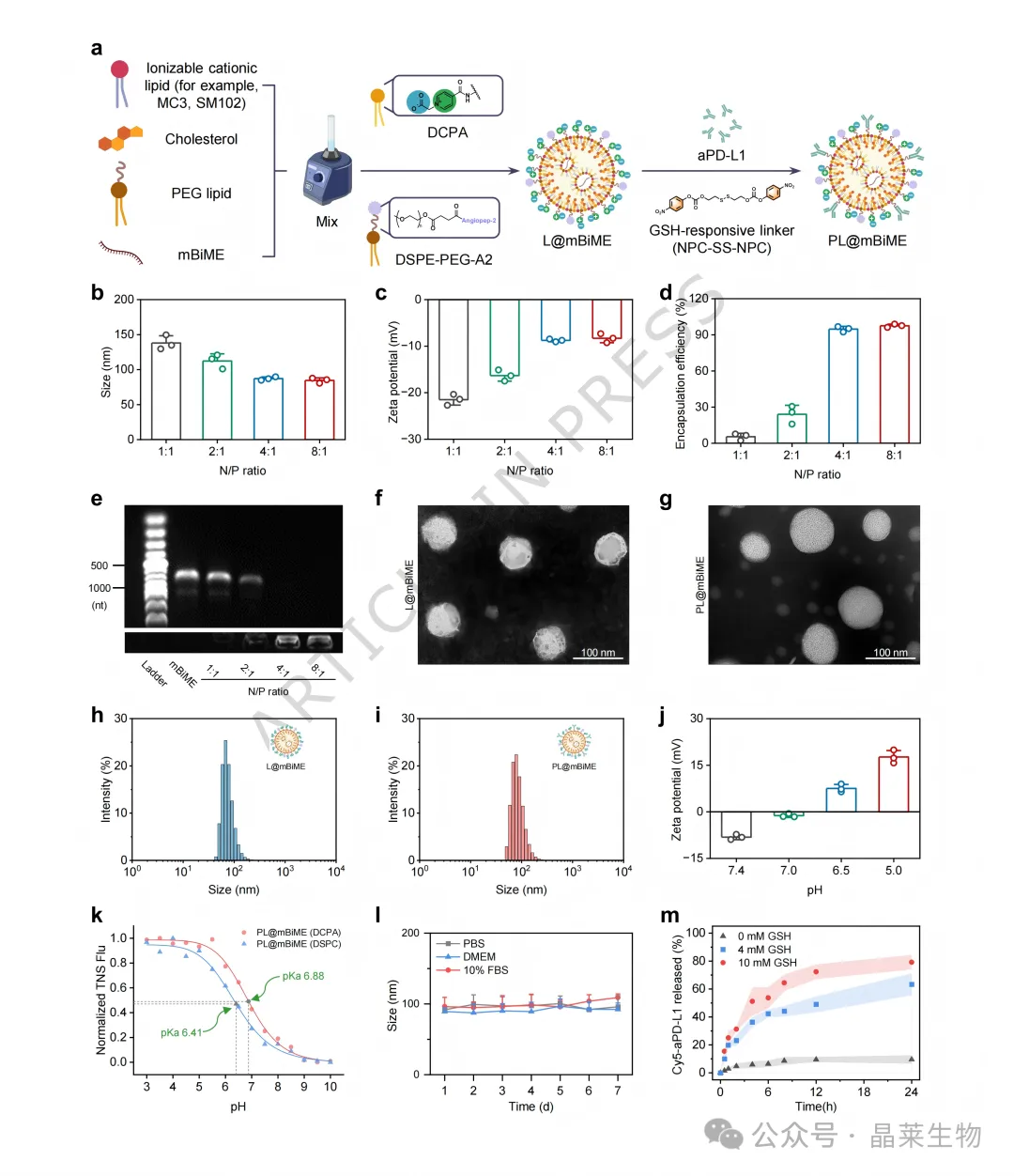
A. PL@mBiME 构建流程;B-D. 不同配比下粒径、电位和 mRNA 包封效率;E. 凝胶阻滞实验验证 mRNA 包载;F-G. 颗粒形态表征;H-I. 粒径分布;J-K. pH 响应性电荷变化;L. 血清稳定性;M. 谷胱甘肽响应性 PD-L1 抗体释放。
3. 酸性环境促进细胞摄取和 mRNA 表达
GBM 肿瘤微环境通常呈偏酸状态。研究团队利用这一特点,提高递送系统在肿瘤区域的响应性。
在中性和酸性条件下分别检测 PL@mBiME 的细胞摄取、内体逃逸和 mRNA 表达情况,以评估 pH 响应结构是否真正转化为递送效率提升。
实验结果显示,在酸性条件下,巨噬细胞和胶质瘤细胞对 PL@mBiME 的摄取均有所增强。颗粒进入细胞后,溶酶体共定位信号下降,说明 mRNA 从内体/溶酶体中逃逸的效率提高。
EGFP mRNA 转染实验进一步验证了无论是在巨噬细胞还是胶质瘤细胞中,酸性环境下均可观察到更强的荧光表达。这说明 PL@mBiME 的酸响应结构并非单纯增加材料设计复杂度,而是直接服务于 mRNA 递送和蛋白表达。
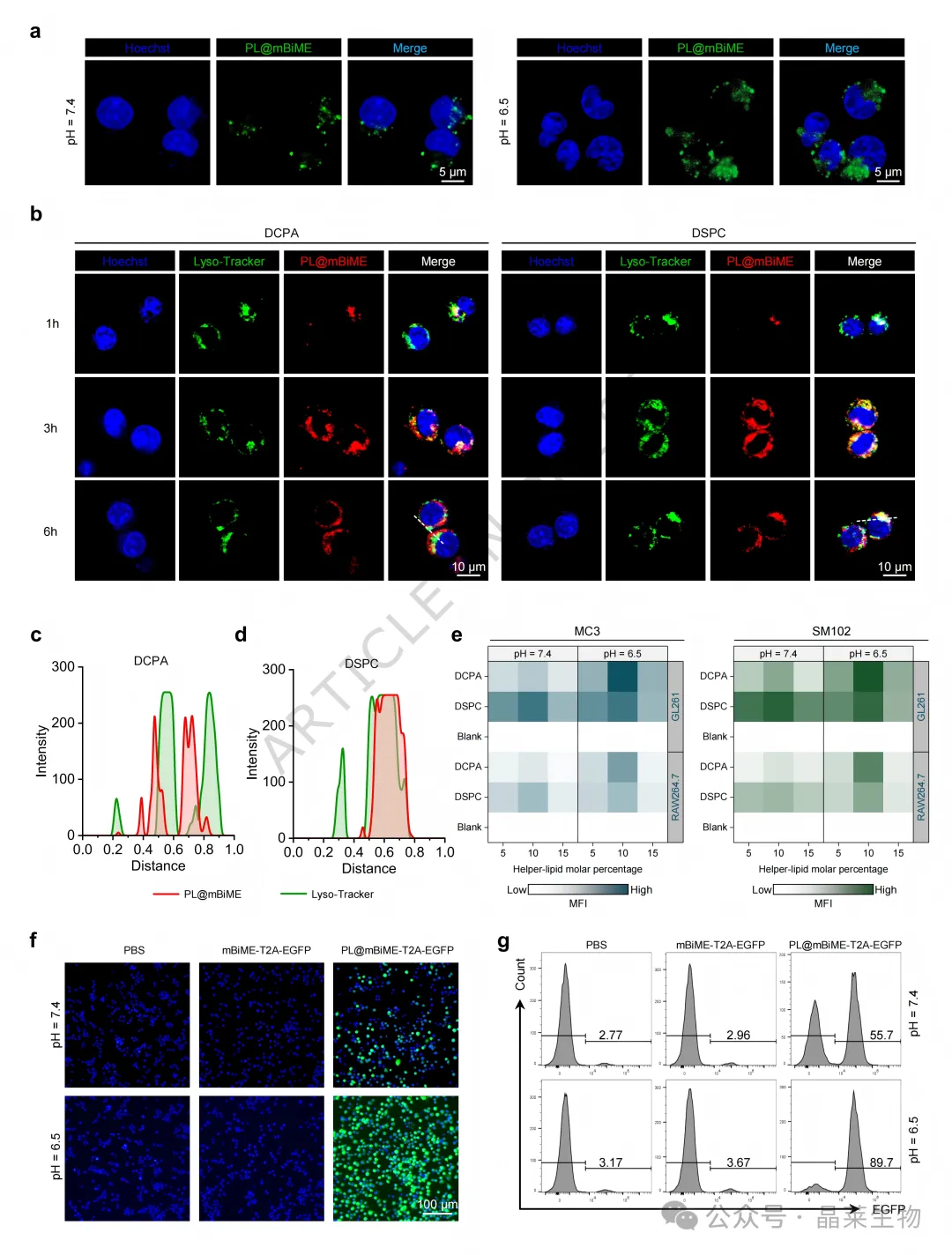
A. 不同 pH 条件下细胞摄取差异;B-D. 溶酶体共定位和内体逃逸分析;E. 细胞内荧光强度变化;F-G. EGFP mRNA 在巨噬细胞和胶质瘤细胞中的表达情况。
4. BiME 连接肿瘤细胞和巨噬细胞,增强吞噬和促炎反应
在确认递送效率后,研究团队进一步评估了 BiME 的免疫功能。
PL@mBiME 进入细胞后表达 BiME,后者同时识别 ErbB2 和 CD206,将胶质瘤细胞与 M2 型巨噬细胞拉近。这样一来,巨噬细胞不再只是肿瘤微环境中的免疫抑制细胞,而是被重新引导参与肿瘤细胞清除。
在巨噬细胞与 GL261 胶质瘤细胞共培养体系中,PL@mBiME 处理后肿瘤细胞被吞噬的比例升高。加入 ErbB2 竞争性阻断后,吞噬增强受到削弱,说明这一过程与 BiME 介导的靶向连接有关。
巨噬细胞表型也同步发生了变化。M1 相关标志物上调,M2 相关标志物下调,促炎因子水平升高,抗炎因子下降。
以上结果显示PL@mBiME 不仅增加了巨噬细胞与肿瘤细胞的接触,也推动巨噬细胞从免疫抑制状态转向更有利于抗肿瘤反应的促炎状态。
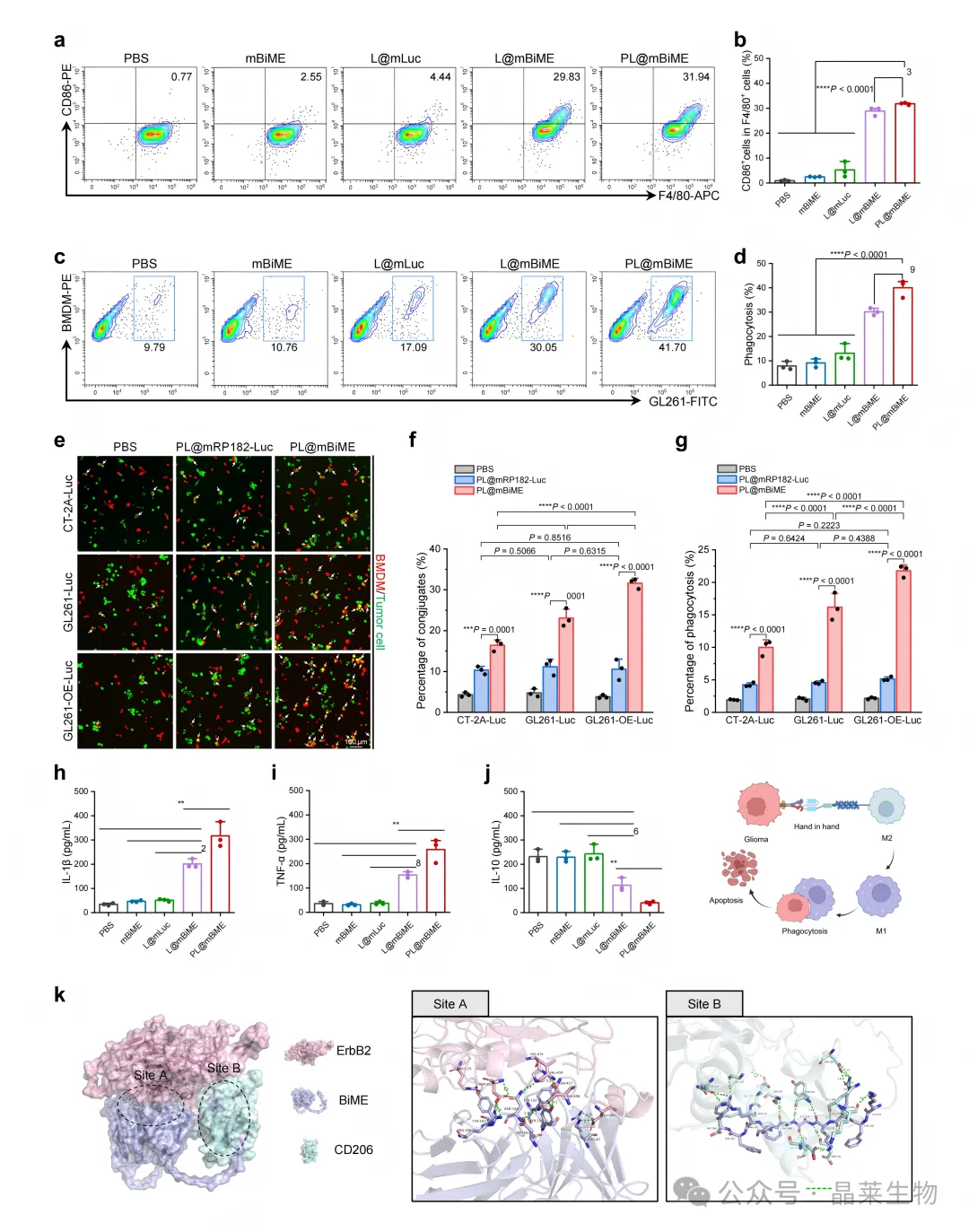
A-B. 巨噬细胞 M1 标志物变化;C-D. 巨噬细胞对 GL261 细胞的吞噬增强;E-G. 不同胶质瘤细胞模型中的吞噬验证;H-J. 炎症因子变化;K. BiME 与 ErbB2/CD206 结合的结构预测;L. 巨噬细胞重编程和吞噬机制示意。
5. PL@mBiME 跨越 BBB 并在脑肿瘤区域富集
脑肿瘤递送绕不开血脑屏障(BBB),即使体外递送效率较高,如果药物无法进入脑部肿瘤,后续免疫调控也难以发生。
为此,研究者建立体外 BBB 模型,并结合小鼠体内成像,评估 PL@mBiME 的脑部递送能力。
在体外 BBB 模型中,PL@mBiME 的穿透能力优于游离抗体和未优化颗粒。进入动物体内后,荧光信号在脑肿瘤区域逐渐增强,并可维持一定时间。离体器官成像结果同样支持其在脑肿瘤区域富集。
这部分结果说明,PL@mBiME 的作用基础并不局限于体外共培养体系。脑靶向设计、酸响应递送和 mRNA 表达共同作用,使该平台具备进入原位脑瘤模型进行疗效验证的条件。
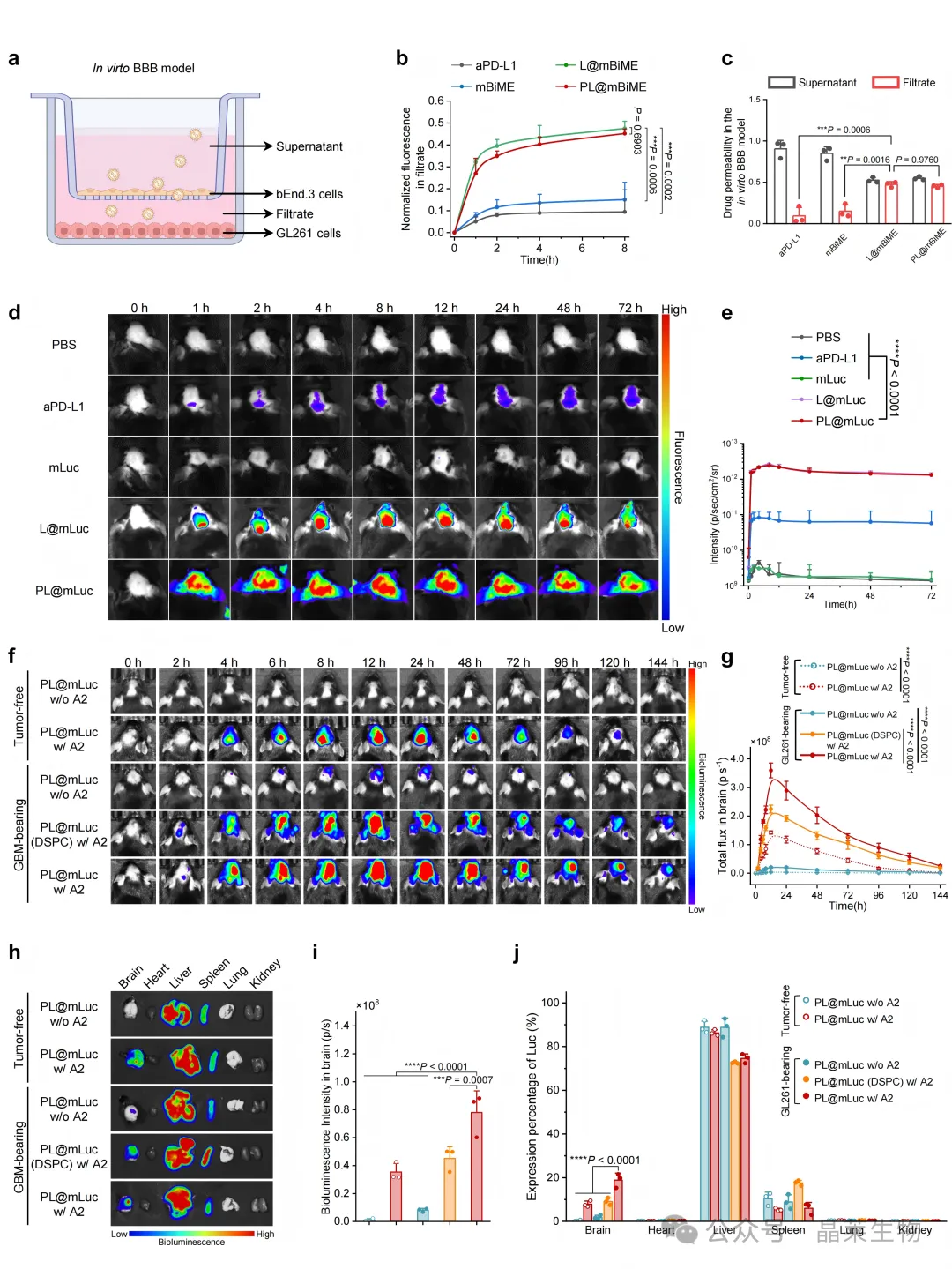
A. 体外 BBB 模型示意;B-C. 不同制剂的 BBB 穿透效率;D-E. 活体成像观察脑部富集;F-G. 脑靶向肽和 pH 响应脂质对递送效果的影响;H-J. 离体器官成像和组织分布定量。
6. 原位 GBM 模型中抑制肿瘤进展,并延长小鼠生存时间
在体内疗效验证实验中研究团队采用原位胶质瘤小鼠模型。与皮下瘤相比,原位脑瘤模型更能体现脑部递送、肿瘤微环境和免疫细胞浸润等因素,也更适合评价 GBM 相关治疗。
在 GL261 原位胶质瘤模型中,PL@mBiME 处理组的肿瘤负荷下降,影像学信号受到抑制,小鼠生存时间延长。与仅递送 mRNA 或单独使用 PD-L1 抗体相比,共递送体系表现出更强的抑瘤效果,显示 BiME 介导的巨噬细胞重编程与 PD-L1 阻断之间存在协同关系。
肿瘤切片显示,Ki67 阳性细胞减少,TUNEL 阳性细胞增加,与影像学观察到的肿瘤进展受抑一致。这说明 PL@mBiME 不仅改变了免疫细胞状态,也在肿瘤组织层面带来了细胞增殖降低和细胞死亡增加。
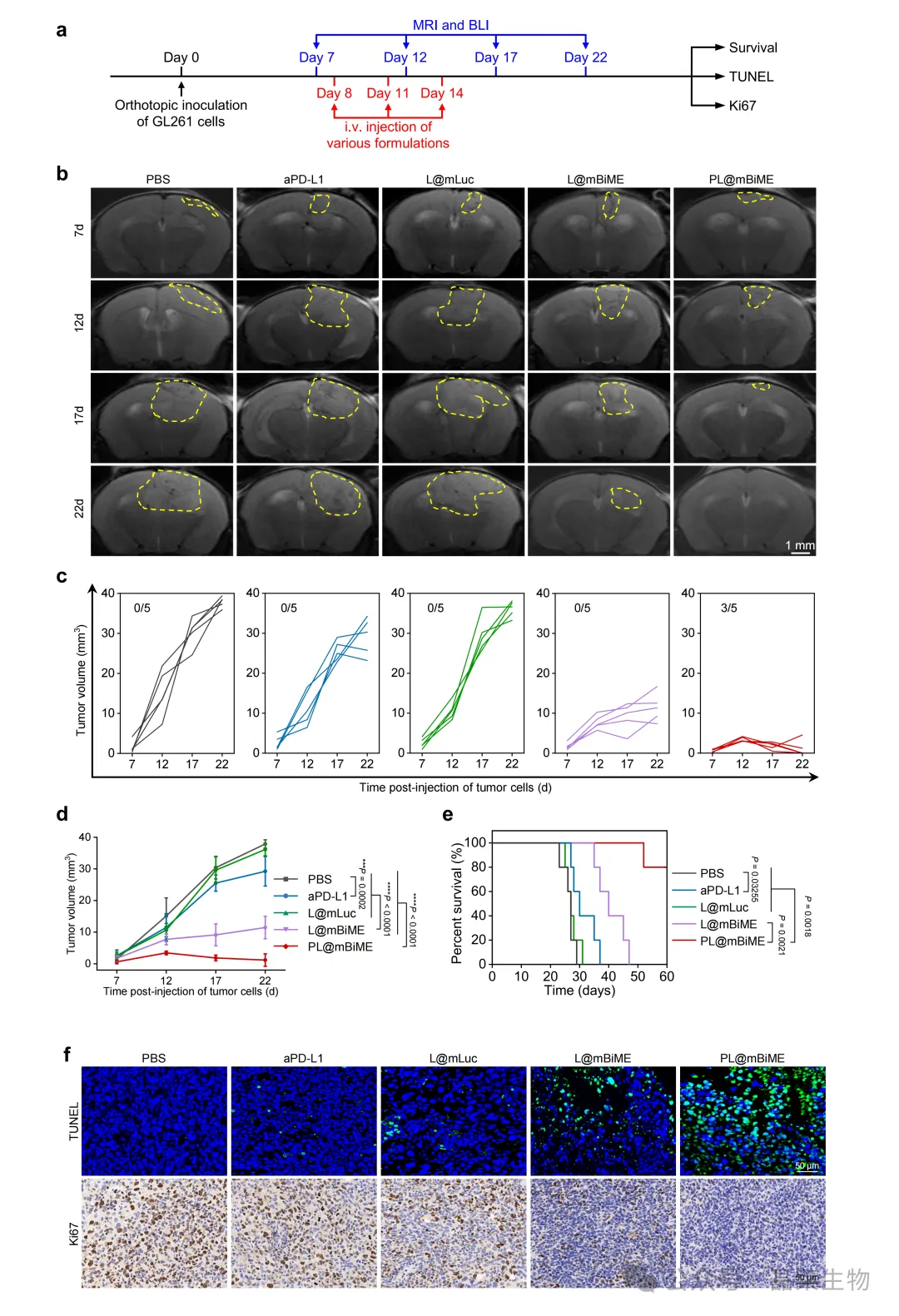
A. 原位 GBM 模型建立与给药流程;B. MRI 观察不同处理组肿瘤变化;C-D. 肿瘤体积变化;E. 小鼠生存曲线;F. TUNEL 和 Ki67 检测肿瘤细胞死亡与增殖。
7. 巨噬细胞重编程带动适应性免疫增强
PL@mBiME 在体内首先改变的是肿瘤相关巨噬细胞。经处理后,肿瘤组织内 M1/M2 比值升高,CD86⁺ 巨噬细胞增加,CD206⁺ 巨噬细胞减少,与体外重编程结果一致。
巨噬细胞表型改变后,肿瘤内 T 细胞组成也随之发生变化。
CD8⁺ T 细胞浸润增加,Treg 比例下降,CD8⁺ T/Treg 比值升高,显示局部免疫环境由抑制状态向抗肿瘤状态转变。DC、NK 细胞和 MDSC 等免疫细胞的变化,也说明 PL@mBiME 对肿瘤免疫微环境的影响并不局限于单一细胞类型。
为了确认关键效应细胞,研究者进行了免疫细胞清除实验。清除巨噬细胞后,PL@mBiME 的抗肿瘤效果明显减弱;清除 CD8⁺ T 细胞后,治疗效果也被削弱。这说明该体系并非单纯依赖 PD-L1 阻断或单一 T 细胞反应,而是通过巨噬细胞重编程带动后续适应性免疫激活。
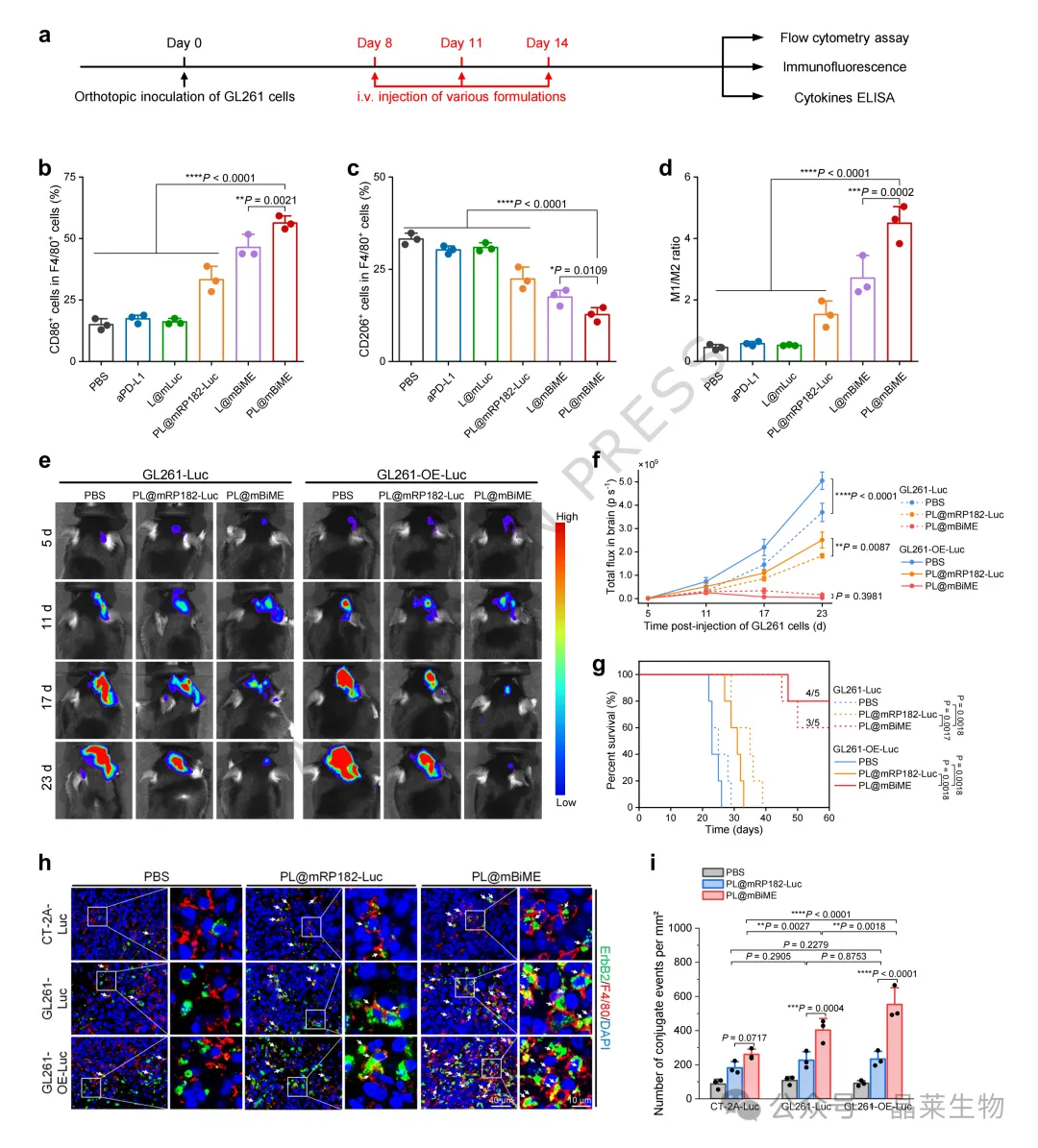
图8 | PL@mBiME 激活先天免疫和适应性免疫
A-F. CD8⁺ T 细胞、Treg 及 CD8⁺ T/Treg 比值变化;G-J. DC、NK 细胞和 MDSC 等免疫细胞变化;K-M. 巨噬细胞或 CD8⁺ T 细胞清除后的肿瘤进展和生存变化。
8. 再次接种显示已形成免疫记忆
除抑制原位 GBM 进展外,研究者同步评估了治疗后是否形成较持久的抗肿瘤免疫。
通过对经 PL@mBiME 治疗并获得肿瘤控制的小鼠进行再次接种,用于观察机体是否能够对同类肿瘤产生更快、更强的免疫应答。
再次接种 GL261 后,PL@mBiME 组小鼠肿瘤生长受到延缓,并延长了小鼠生存时间。脾脏、脑组织和引流淋巴结中的记忆性 CD8⁺ T 细胞比例升高,显示治疗后机体形成了一定程度的免疫记忆。
本部分实验结果显示:PL@mBiME 不仅在给药期间增强巨噬细胞和 T 细胞抗肿瘤作用,还可能帮助机体建立后续免疫防御。
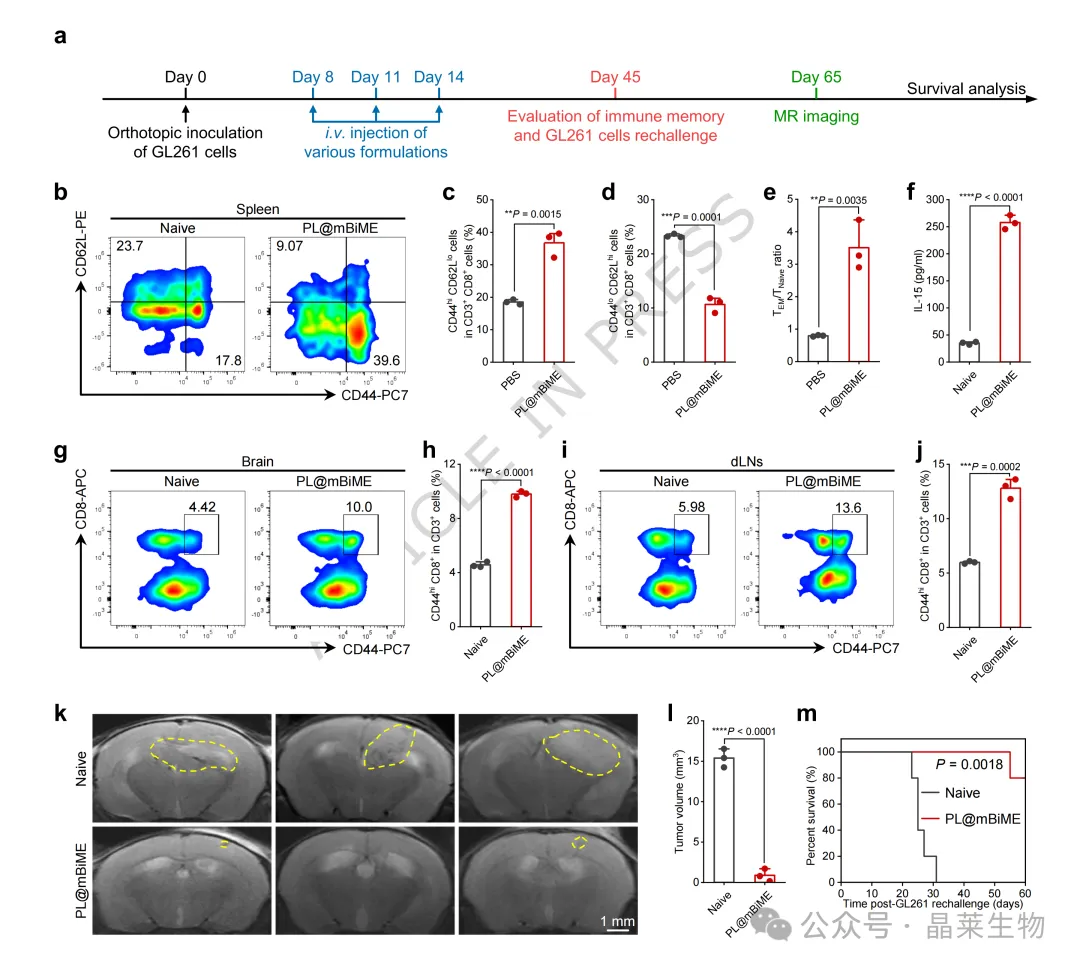
A. 治疗和再次接种流程;B-F. 脾脏效应记忆 T 细胞及相关因子变化;G-J. 脑组织和引流淋巴结中记忆性 CD8⁺ T 细胞变化;K-M. 再次接种后 MRI、肿瘤体积和生存曲线。
该研究的意义在于将脑肿瘤递送、巨噬细胞重编程和 PD-L1 阻断放入同一个 LNP 系统中。
与单独递送抗体或单独调节某类免疫细胞相比,PL@mBiME 更强调在脑肿瘤局部同时完成递送、识别、吞噬和 T 细胞激活。也为 GBM 免疫治疗提供了不同于传统 T 细胞中心策略的研究思路。GBM 中本就存在大量肿瘤相关巨噬细胞,但其中不少处于免疫抑制状态。
通过 BiME 将巨噬细胞与肿瘤细胞连接起来,并推动其向促炎表型转变,研究团队尝试把肿瘤微环境中的“存量细胞”重新纳入抗肿瘤反应。
该研究展示了 mRNA/LNP 在肿瘤免疫调控中的应用潜力。相比直接给药蛋白类衔接器,mRNA 可在体内表达目标分子;配合脑靶向和肿瘤响应型递送设计,有助于提高脑肿瘤区域的局部作用。
结语
本研究开发了一种肿瘤微环境响应性脂质纳米颗粒PL@mBiME,通过共递送编码双特异性巨噬细胞衔接器的mRNA和PD-L1抗体,实现了跨越血脑屏障、靶向胶质母细胞瘤、重编程肿瘤相关巨噬细胞为M1表型、促进巨噬细胞吞噬肿瘤细胞、激活CD8⁺ T细胞抗肿瘤免疫的多重功能。
在多种原位GBM模型中,PL@mBiME诱导了显著的肿瘤消退和长期免疫记忆,且具有良好的生物安全性。该策略为胶质母细胞瘤及其他ErbB2⁺、巨噬细胞富集型恶性肿瘤提供了新的免疫治疗范式。
关于晶莱















