聚焦肿瘤类器官:连接癌症基础研究与临床治疗的关键模型!
时间:2026-03-09 阅读:232
肿瘤类器官的构建
目前已有多个研究成功从结直肠癌、胰腺癌、乳腺癌、肝癌等多种上皮源性肿瘤(含原发灶和转移灶)构建类器官库,部分库还包含患者配对的正常组织类器官,建系效率因癌症类型不同存在差异(如结直肠癌~90%-100%,前列腺癌仅~15%-20%);
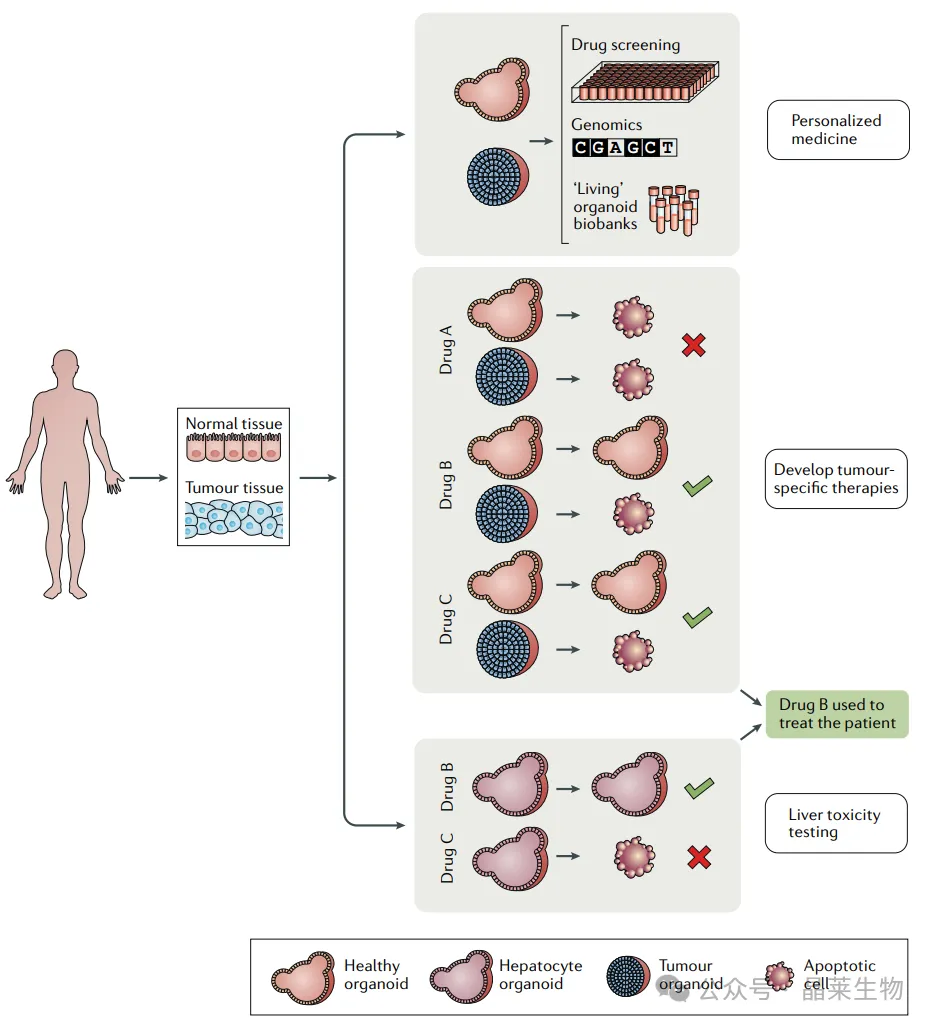
用于个体化癌症治疗与药物研发的类器官培养体系
上图:类器官可从患者来源的正常组织与肿瘤组织样本中构建。
中图:对类器官培养物进行遗传学鉴定后,可用于药物筛选,从而建立肿瘤遗传背景与药物反应的关联。类器官可经冻存,保存在活体类器官生物样本库中。构建同一患者正常组织来源类器官。
下图:可筛选能特异性杀伤肿瘤细胞、而不损伤正常细胞的化合物,从而研发毒性更低的药物。可自我更新的肝细胞类器官培养体系,可用于检测潜在新药的肝毒性——这是导致药物在临床试验中失败的原因之一。
构建时需通过选择性培养条件(如去除 WNT、EGF,使用 nutlin-3)排除正常组织类器官的过度生长,保证肿瘤类器官的纯度;
这类生物样本库可实现肿瘤遗传背景与药物反应的关联分析,还能为蛋白质组学、转录组学等多组学研究提供模型,目前全球已启动人类癌症模型计划(HCMI),构建全球可及的类器官资源库。
类器官在癌症基础研究中的重要价值
1. 类器官为癌症基础研究提供了接近体内环境的体外模型,填补了传统模型在机制研究中的空白,核心应用包括:
探索病原体与癌症发生的关联:构建病原体 - 类器官共培养模型,研究幽门螺杆菌、肠炎沙门氏菌、肝炎病毒等病原体介导肿瘤发生的机制,如胃类器官揭示幽门螺杆菌的定植和致炎机制,胆囊类器官证实沙门氏菌通过激活 AKT/MAPK 通路诱导细胞恶性转化;
2. 解析肿瘤发生的突变过程
① 利用正常类器官的遗传稳定性,揭示器官特异性突变特征(如肠干细胞因快速增殖发生脱氨基诱导的 C>G 至 T>A 转换),明确突变过程与肿瘤驱动基因突变的关联;
② 通过克隆性类器官培养,分析肿瘤的瘤内异质性,发现肿瘤进展中突变率会显著升高,且治疗前已存在耐药克隆,为耐药机制研究提供依据;
③ 利用 CRISPR-Cas9 编辑类器官,可明确 DNA 修复基因缺陷与突变特征的因果关系,为肿瘤分子诊断提供标志物。
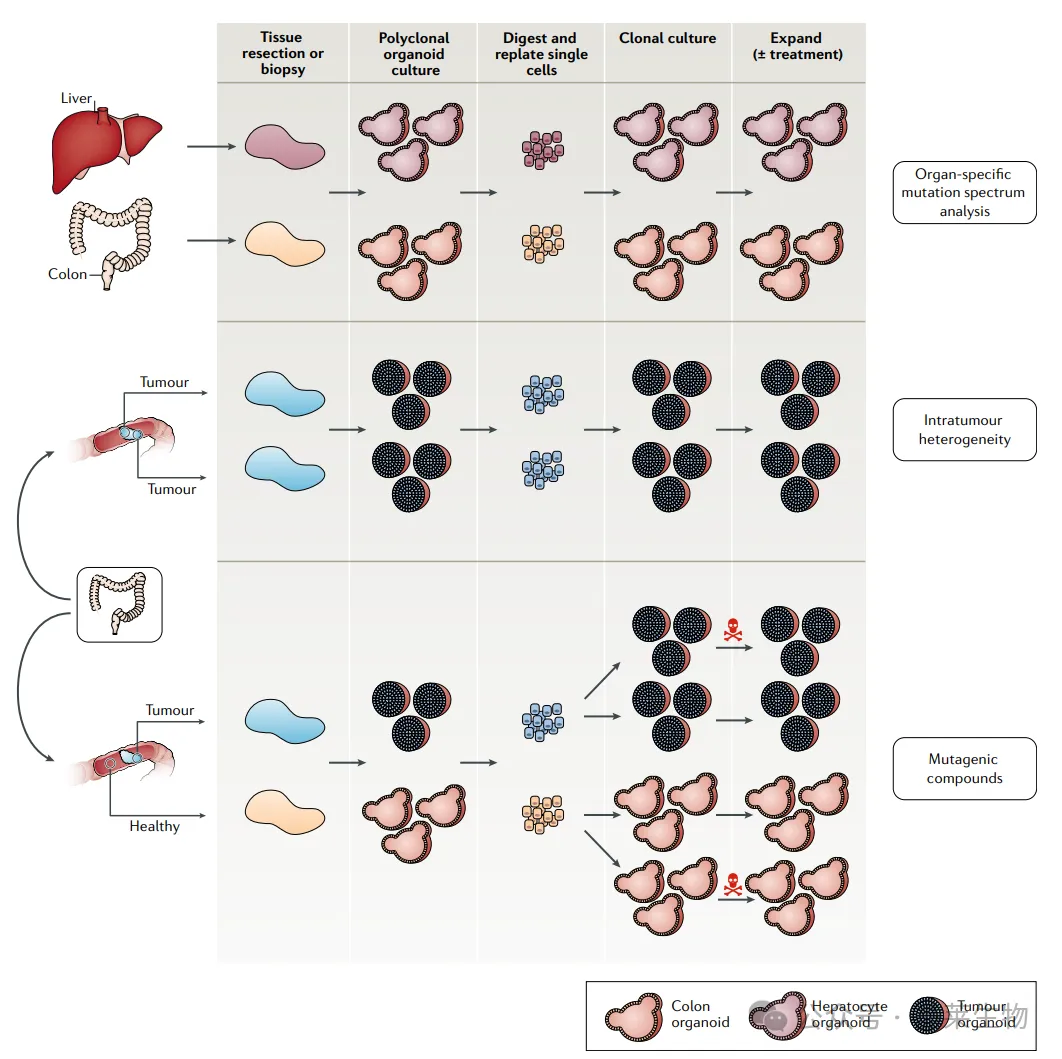
用于解析肿瘤发生相关突变过程的类器官培养体系
上图:从不同正常器官中培养克隆性类器官,随后对培养物进行全基因组测序,可解析器官特异性的突变谱。
中图:通过培养同一肿瘤不同区域来源的克隆性类器官,可利用类器官研究瘤内异质性。
下图:对克隆性培养物进行全基因组测序,可揭示区域特异性的突变谱。利用与上述类似的方法,类器官培养体系可用于研究特定化合物对正常细胞与肿瘤细胞突变谱的影响。
3. 癌症的遗传建模与机制研究
① 以正常类器官为基础,通过基因编辑导入癌症驱动突变,构建结直肠癌、胰腺癌等癌症的进展模型,揭示突变组合对肿瘤发生、转移的影响(如 APC+TP53 缺失导致染色体不稳定性,四突变组合可诱导浸润性腺癌);
② 证实原位移植是研究肿瘤转移的关键,皮下移植的类器官肿瘤无法自发转移,而原位移植可重现肝、肺转移,且癌症干细胞(CSC)是转移灶形成和维持的核心;
③ 用于研究癌症相关信号通路(如 WNT、TGFβ)的调控机制,明确关键基因突变(如 RNF43、BRAF^V600E)在肿瘤发生中的作用,为靶向治疗提供靶点。
类器官在癌症药物研发和治疗中应用
1. 药物研发与个体化癌症治疗
① 类器官能更好地重现原发肿瘤特征,弥补传统二维模型的不足,其低 / 高通量药物筛选已在小规模研究中取得良好结果,对转移性胃肠道癌的药物预测阳性值达 88%、阴性值达 100%;
② 可揭示药物耐药的遗传 / 表观遗传机制,为治疗方案分层提供依据,还能同时利用患者正常和肿瘤类器官,筛选肿瘤特异性药物,降低治疗毒性(如利用肝细胞类器官检测药物肝毒性);
③ 已在结直肠癌、前列腺癌、肝癌等癌症中实现临床药物测试和治疗方案优化,甚至为部分难治性癌症找到潜在治疗靶点(如 ERK 抑制剂用于肝癌)。
2. 免疫治疗的研究与应用
① 解决了免疫治疗中肿瘤免疫原性研究和免疫细胞体外扩增的问题,可构建类器官与免疫细胞的共培养体系(如 IEL、CD45 + 淋巴细胞、Vδ2+ T 细胞),实现免疫细胞的体外维持和功能保留;
② 可检测健康供体来源 T 细胞对患者肿瘤类器官的细胞毒性,为过继性细胞治疗提供候选细胞,胸腺类器官的研发还为肿瘤特异性 T 细胞的扩增提供了更生理的模型。
类器官癌症研究的发展前景与优化方向:
1. 培养体系优化:研发合成基质替代小鼠来源 ECM,开发水溶性 WNT 激动剂、脂质稳定 WNT 蛋白等技术,实现类器官的无血清培养,降低外源性因素干扰;
2. 模型复杂性提升:构建整合基质细胞、免疫细胞、微生物的共培养体系,研发具有功能性神经系统、血管的类器官,复刻更接近体内的肿瘤微环境;
3. 技术拓展:推进非上皮源性肿瘤的类器官培养技术,利用类器官开展化疗、放疗的诱变机制研究,为降低治疗副作用、减少第二原发肿瘤风险提供依据;
4. 临床转化落地:进一步验证类器官对肿瘤药物反应的预测价值,优化药物筛选平台的灵敏度和稳定性,推动类器官技术在个体化医疗、肿瘤诊断中的临床应用,目前其在囊性纤维化中的诊断应用已得到验证,癌症领域的临床试验正在开展。
晶莱生物类器官解决方案
小晶有丰富的类器官实战经验和成熟的技术检测平台,能帮您用好类器官,理清思路,少走弯路,多出成果。类器官研究遭遇瓶颈?晶莱生物为您提供专业解决方案!
如果您:苦于类器官培养重复性差、生长状态不稳定;在机制验证与药物筛选中陷入困境,无法推进;缺乏体内外转化研究经验,不知如何衔接基础与临床;晶莱生物类器官专家团队,正是您需要的科研伙伴!
我们提供:
①标准化类器官培养体系——浓度、温度、操作SOP全搞定,拒绝批次差异;
②基质胶优化支持——不同类型类器官匹配最适胶条件,不飘不贴不散胶;
③全流程技术服务——从原代构建到药筛检测,帮你多、快、好、省地拿到结果;
④专家一对一支持——培养不出、表型不对、结果不重复?我们直接帮你排查!
关于晶莱















