从肾脏发育到类器官血管化:一篇读懂最新研究进展与挑战!
时间:2026-04-27 阅读:109
肾脏类器官无论是作为器官研究模型,还是再生医学的细胞来源,都有望极大推动肾脏病学领域的发展。尽管目前在重现肾脏器官特异性细胞谱系方面已取得重大进展,但血管化仍是该领域亟待突破的核心瓶颈。尤其是肾小球血管化——这一肾脏生理功能不可或缺的关键环节,在体外培养体系中极少能成功实现。综述Kidney organoid vascularization: current advancements in the field系统总结了肾脏类器官血管化领域的现有研究成果。

1.三阶段肾发生
哺乳动物肾脏依次经历前肾→中肾→后肾,最终后肾发育为永久肾。
人:妊娠第5周启动后肾发生;小鼠:E10.5
肾发生在人约36周停止,小鼠出生后3–5天停止。
2.两大起源结构
①输尿管芽(UB):发育为集合管、肾盂、输尿管。
②后肾间充质(MM):发育为全部肾单位(足细胞、近端小管、亨利袢、远端小管)。
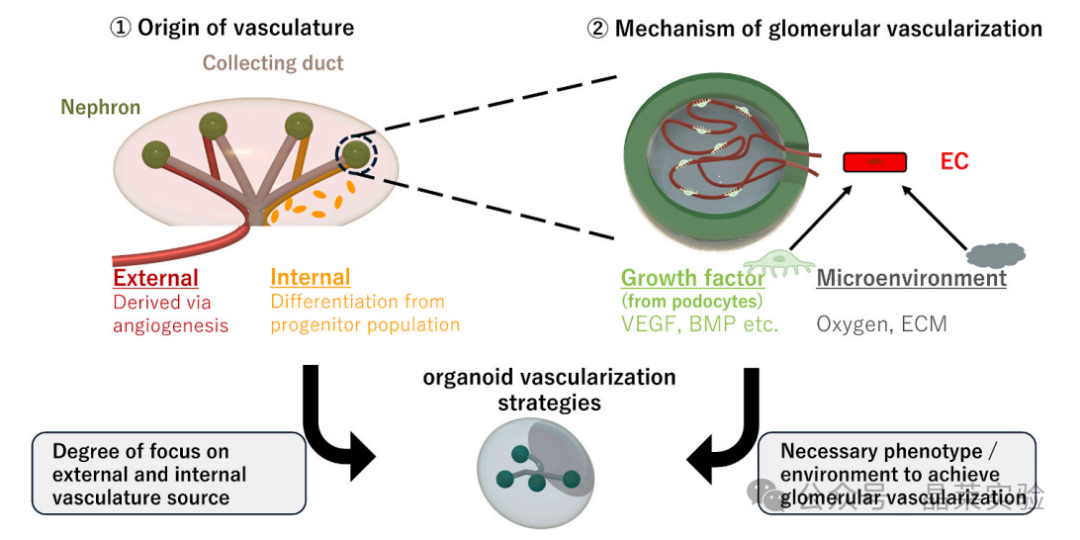
①脉管系统的起源;②肾小球血管化的发生机制
3.关键调控轴
①GDNF/RET:引导输尿管芽出芽与分支。
②Wnt9b/β-catenin:启动肾单位分化。
③Six2:维持肾单位祖细胞干性。
④Foxd1+间质:分化为周细胞、系膜细胞,调控血管排布。
血管发育两条核心路径
内皮来源:中间中胚层原位分化+主动脉血管芽生共同参与。
肾小球血管化关键信号:
VEGF(足细胞分泌):招募内皮、维持窗孔。
BMP4、Ang1、Sema3A/3C:精细调控血管形态与稳定。
PDGFβ:招募系膜细胞,支撑肾小球血管。
肾小球血管化是肾脏功能的前提,依赖足细胞—内皮—系膜的时空精确对话,这是体外最难复刻的环节。
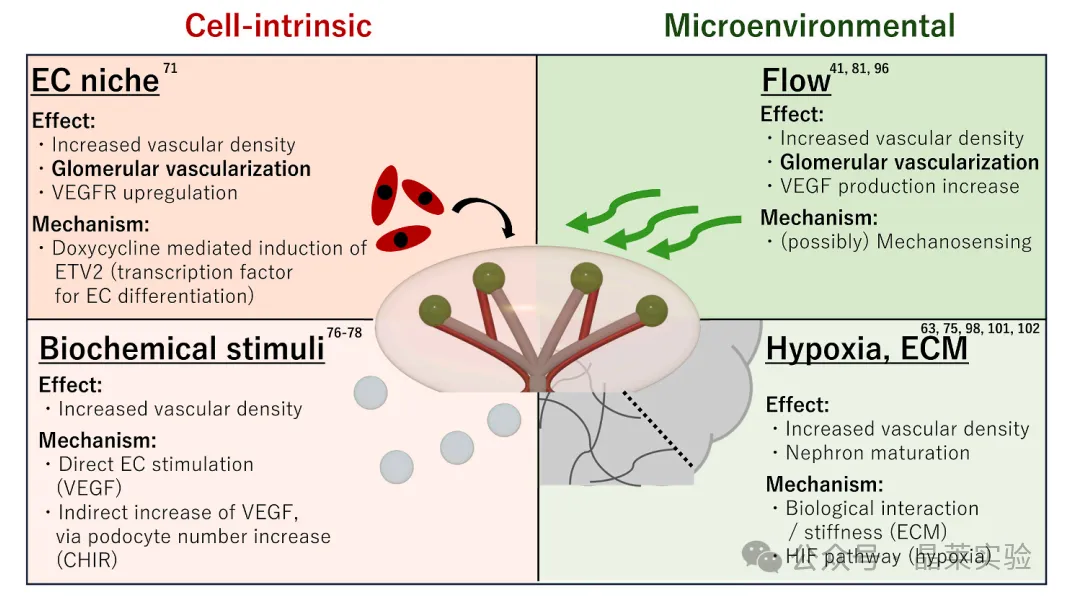
1.体内移植介导的血管化(当前最成熟、最有效)
①方法:肾被膜下移植、鸡胚CAM移植、淋巴结移植。
②优势:宿主血管侵入,稳定实现肾小球血管化。足突、内皮窗孔、基底膜成熟。可作为体外策略的“阳性对照”。
③局限:通量低、异种嵌合、伦理与临床转化限制。内皮来源存在争议:宿主为主/供体为主/混合。
2.增强内源性血管生成:细胞内在策略
①ETV2诱导内皮龛(最成功的基因工程手段)
多能干细胞可诱导ETV2→强力分化为内皮。
与野生型细胞共聚集→形成动脉/静脉/肾小球内皮。
实现体外肾小球血管化,内皮出现窗孔结构。
机制:提升VEGFR表达,而非直接升高VEGF。
②生化因子调控
VEGF直接添加:扩增内皮,但不实现肾小球血管化。
缩短CHIR暴露:提高肾小球/小管比例→足细胞增多→VEGF总量上升→血管密度增加。
专家结论:VEGF是必要非充分条件,肾小球血管化需要内皮表型与微环境协同。
3.增强内源性血管生成:微环境策略
①流体剪切力与机械感知(体外唯一实现肾小球血管化)
微流控灌注/悬浮搅拌→机械力驱动血管化。
机制:Integrinα2β1机械感受器激活;系膜细胞、内皮共同参与;上调VEGF与VEGFR,促进肾小球血管侵入。
关键:流动≠营养输送,机械信号本身是核心驱动。
②细胞外基质(ECM)硬度与成分
硬度1000–5000Pa最优(模拟肾/CAM)。
肾脏脱细胞ECM:生化信号+结构支持,显著促血管化。
结论:ECM同时提供力学信号与生物配体,缺一不可。
③生理性低氧(7%O₂)
通过HIF通路提升VEGF亚型,增加微血管密度。
不损害肾单位发生。
关键:氧分压时序比浓度更重要。
4.与外部脉管系统连接的相关研究探索
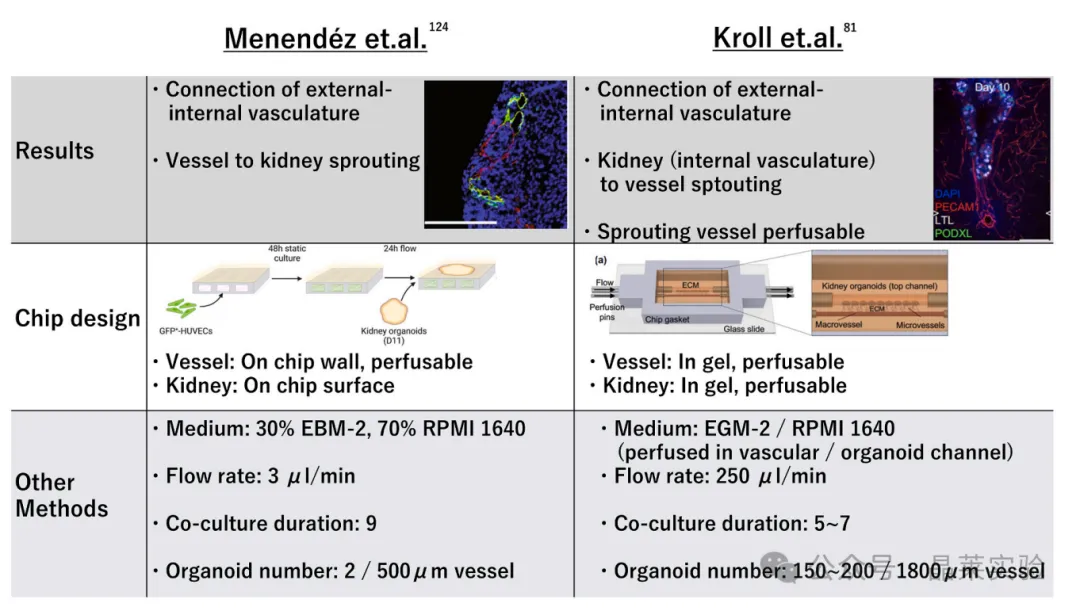
外部血管网络(HUVEC)+类器官共培养,实现内外血管连通与灌注。
问题:额外VEGF可能干扰肾小球内源性梯度!!培养基不兼容导致纤维化。
未来:共灌注、共培养基、共机械刺激三同步。
可用于未来技术整合的替代策略
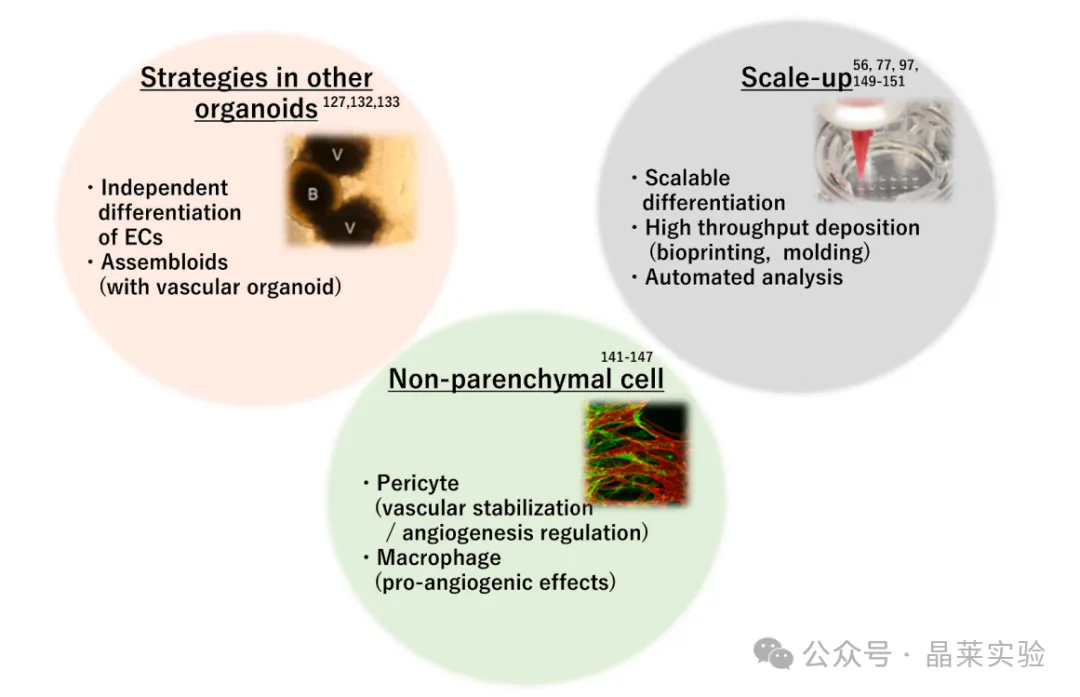
1.其他类器官血管化经验
①独立分化器官特异性内皮,再共组装。
②组装类器官(Assembloid):肾脏类器官+血管类器官融合。
③借鉴肝、脑类器官的器官特异性内皮特化方案。
2.引入非实质细胞
①周细胞:稳定血管、调控管径、抑制异常出芽。
②巨噬细胞:促血管生成、支持发育性血管连接。
目前肾脏类器官普遍缺失,是成熟度低的重要原因。
3.规模化与高通量
①悬浮培养、3D生物打印、蜂窝状膜培养→尺寸均一、可放大。
②自动化分化与分析→降低批次差异,利于药物筛选。
1.转化壁垒
①功能不完整:无尿液引流通道、无成熟滤过、无球管反馈。
②成熟度停留在胎儿阶段:血管仅部分开窗、肾小球结构简化。
③异质性与可重复性差:批次间血管化程度差异大。
④体外无法长期维持灌注:静态培养中心坏死,流动系统复杂昂贵。
2.安全性问题
①脱靶细胞风险:神经细胞、软骨细胞等非肾细胞混杂,移植有致畸/肿瘤风险。
②免疫排斥:异体内皮/基质引发排斥;自体iPSC-EC是方向。
③血管失控增生:高VEGF、ETV2持续表达可能导致血管畸形。
④嵌合与伦理:体内移植产生人—动物嵌合血管,监管严格。
肾脏类器官血管化的核心是复刻发育:以内皮龛 / ETV2 提供细胞来源,以流体 / ECM / 低氧提供微环境,以足细胞 — 内皮 — 系膜对话实现肾小球特异性血管化;最终要走向体外可灌注、可成熟、可放大、可安全移植的一体化工程化体系。
关于晶莱














