Nature 子刊重磅|类器官化身术后“活体药仓”,能否同时实现乳腺癌控复发与乳腺再生?
时间:2026-04-28 阅读:106
写在前面
乳腺癌术后管理需要同时面对两类问题:术区残留微小病灶可能引发局部复发,肿瘤切除造成的组织缺损也会影响乳腺结构、外观重建及部分生理功能。
现有局部递药体系多聚焦于“控复发”,组织工程策略则主要用于“补缺损”,二者尚难整合为兼具治疗和再生功能的一体化方案。

2026年4月17日,浙江大学顾臻、俞计成、山东大学胡慧丽、苏州大学王慎强共同通讯发表于《Nature Biomedical Engineering》(IF=26.7)的一项研究围绕这一问题提出了工程化乳腺类器官 depot 策略。
研究团队将乳腺类器官诱导至泌乳样状态,使其形成可装载亲脂性前药的脂滴结构,并利用肌上皮细胞收缩释放含药脂滴,在术后局部持续发挥化疗作用。与此同时,植入类器官还能与宿主乳腺组织整合,参与导管样结构重建,并在动物模型中支持泌乳功能恢复。
该研究将乳腺类器官的分泌功能、细胞组成和再生潜能整合到同一平台中,使其从体外建模和药物筛选工具,进一步拓展为可植入、可递药并参与组织重建的活体工程单元。
1. 构建具备泌乳样功能的工程化乳腺类器官 depot
研究者分别以小鼠乳腺类器官和人 iPSC 来源乳腺类器官为基础,诱导其获得泌乳样表型并形成脂滴结构。在此基础上,研究团队利用亲脂性 pH 响应前药 ATRA-DOX 的理化特征,将其富集于类器官脂滴内,形成工程化乳腺类器官 eMO/eHMO。
2. 利用乳腺类器官的内源性分泌与收缩行为实现局部递药
该体系将脂滴作为前药储存空间,并借助肌上皮细胞收缩促进含药脂滴排出。残留肿瘤细胞摄取脂滴后,ATRA-DOX 可在酸性微环境中裂解释放 DOX,从而增强局部细胞毒作用。
3. 在乳腺癌术后复发模型中验证抗复发作用
在小鼠术后乳腺癌模型中,预装载 ATRA-DOX 的工程化乳腺类器官较游离药物、前药以及“类器官+药物”简单混合处理表现出更强的复发抑制效果。该结果对支持类器官介导的装载、滞留与释放过程对疗效提升具有实质论证作用。
4. 将局部治疗与乳腺组织再生纳入同一工程体系
植入后的乳腺类器官并非单纯停留在术区作为药物释放载体,而是能够与宿主乳腺组织发生整合,参与导管样结构重建。在妊娠和分娩相关动物模型中,研究者还观察到乳腺泌乳功能恢复,表明该体系具有一定的功能性再生潜力。
5. 人 iPSC 来源乳腺类器官提供初步转化验证
研究团队进一步构建人 iPSC 来源乳腺类器官,并验证其在前药装载、泌乳样释放、术后抗复发和组织再生方面的功能。该部分实验为自体或个体化来源类器官的后续研究提供了概念依据。
1. 具备泌乳样功能的乳腺类器官构建与鉴定
研究者首先建立乳腺类器官培养体系,并对其细胞组成和组织样结构进行表征。培养获得的类器官包含腔面上皮细胞和肌上皮细胞等乳腺上皮关键细胞类型,能够形成类似导管结构的三维组织形态,为后续递药和再生实验提供了细胞基础。
在泌乳诱导条件下,乳腺类器官内出现脂滴积累,并伴随分泌相关标志物表达变化,说明该体系能够在体外获得一定程度的泌乳样功能。
GFP 标记类器官移植结果表明植入细胞可参与宿主乳腺导管样结构形成,显示其作为活体 depot 进行局部递药和组织重建的可行性。
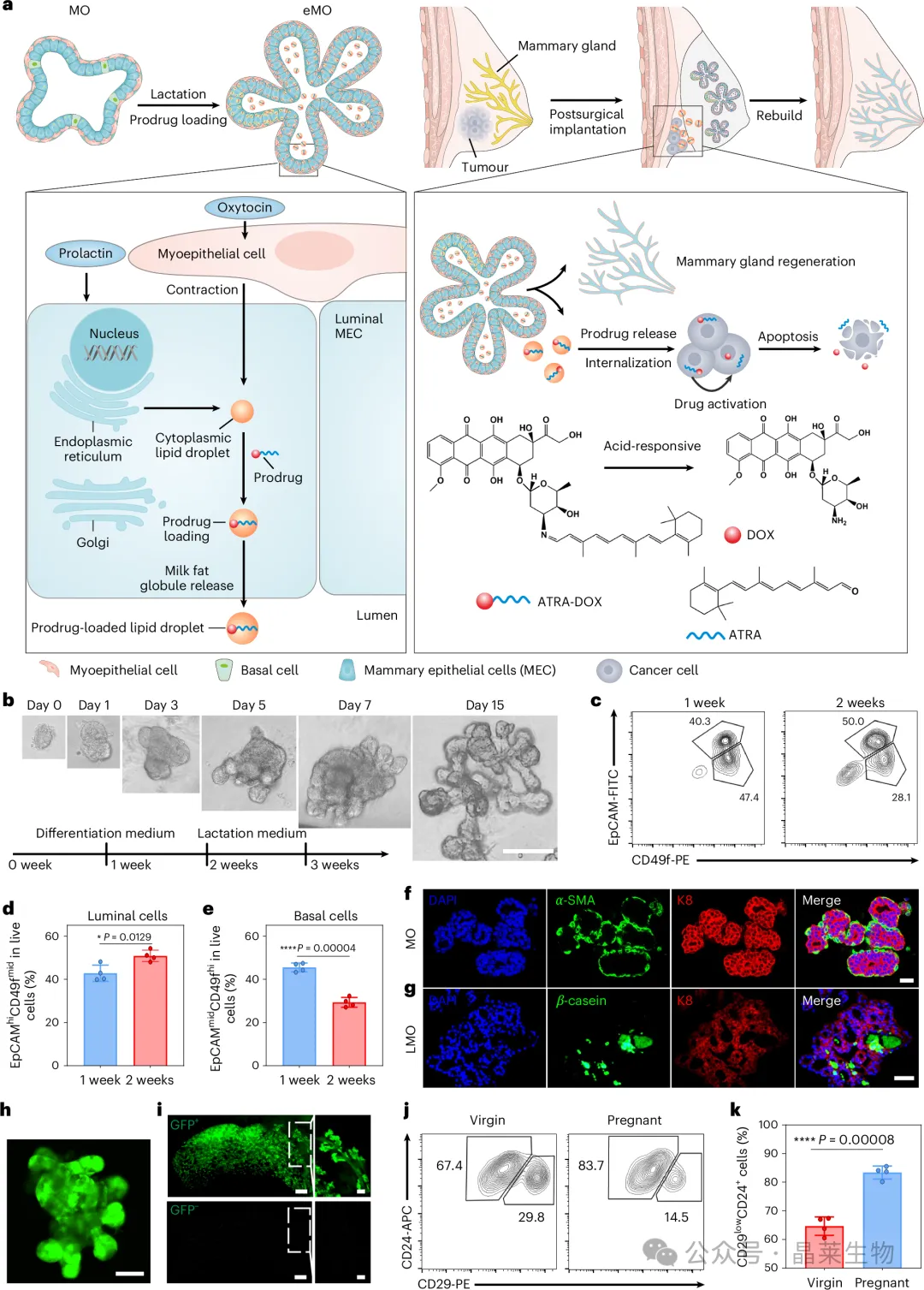
图1 | 工程化乳腺类器官 depot 的构建思路与乳腺类器官基础表征 A. 研究总体设计:乳腺类器官构建→泌乳样诱导→前药装载→术后局部植入→抗复发与组织再生;B. 乳腺类器官形态及乳腺上皮标志物表达;C. 泌乳诱导后脂滴形成及分泌相关标志物变化;D. GFP 标记类器官体内植入后参与乳腺导管样结构形成;E. 工程化乳腺类器官用于局部化疗和腺体再生的模式图。
2. ATRA-DOX 前药装载与工程化乳腺类器官的构建
为提高类器官的载药效率和局部释放可控性,研究者设计了由 all-trans retinal 与 doxorubicin 组成的 pH 响应性前药 ATRA-DOX。相较于游离 DOX,ATRA-DOX 具有更强亲脂性,更适合进入泌乳样类器官产生的脂滴结构。
荧光共定位实验结果显示,ATRA-DOX 与脂滴信号具有较高重叠度,而游离 DOX 与脂滴的共定位程度较低。定量分析进一步显示,泌乳样乳腺类器官的载药效率高于普通乳腺类器官,说明脂滴积累是该体系获得较高药物负载能力的重要前提。
释放实验表明,工程化乳腺类器官能够持续释放药物,并在酸性条件下增强 DOX 释放。该设计与肿瘤局部微环境偏酸性的特点相匹配,但需要区分的是,酸敏裂解并不等同于严格的肿瘤特异性释放,其主要作用在于提高酸性环境中的前药裂解效率。
在体外杀伤实验中,未装药类器官对 4T1 乳腺癌细胞的直接抑制作用有限;装载 ATRA-DOX 后,工程化乳腺类器官能够明显诱导肿瘤细胞死亡。由此可见,该体系的抗肿瘤效应主要来自类器官介导的前药储存和释放,而非类器官本身的非特异性细胞毒作用。
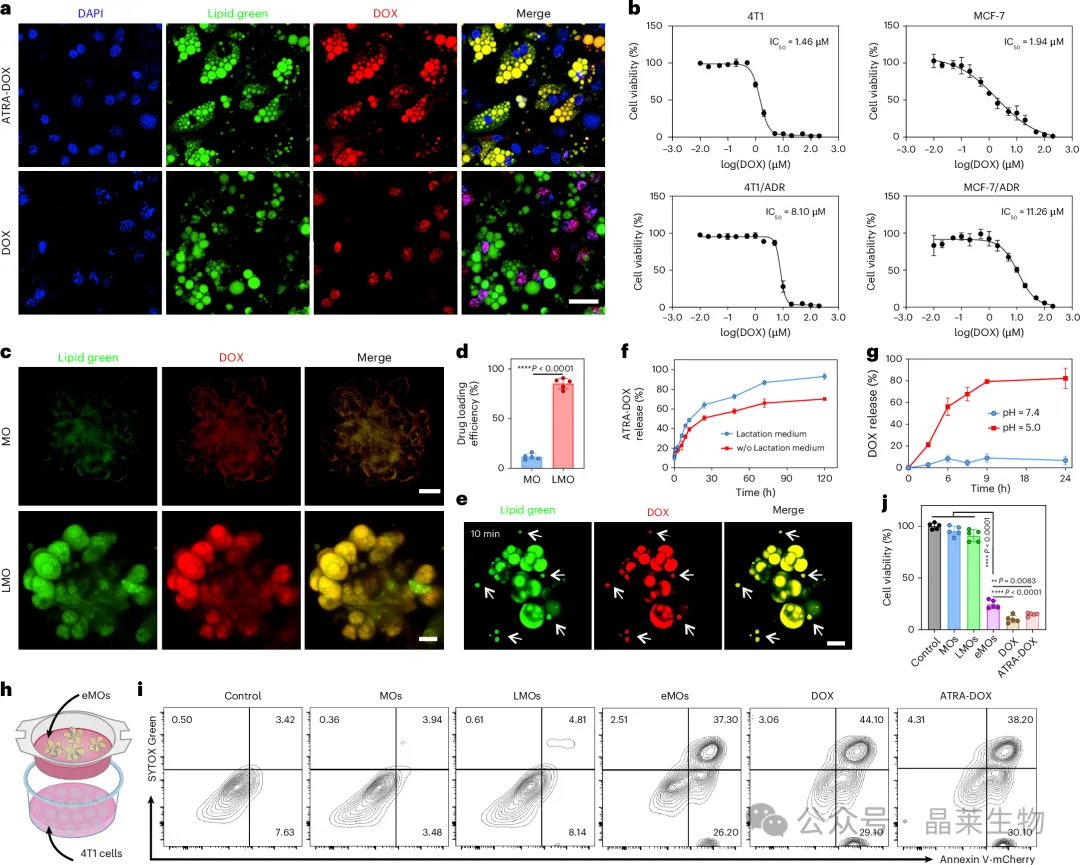
图2 | 工程化乳腺类器官的前药装载、释放与体外抗肿瘤活性 A. 游离 DOX 与 ATRA-DOX 在乳腺类器官脂滴中的分布差异;B. ATRA-DOX 与脂滴共定位分析;C-D. 普通乳腺类器官与泌乳样类器官的载药效率比较;E. 工程化乳腺类器官结构示意;F-G. 不同 pH 条件下前药释放及 DOX 释放曲线;H-J. 工程化乳腺类器官对乳腺癌细胞的体外杀伤效果。
3. 工程化乳腺类器官在术后复发模型中抑制肿瘤再生长
在完成体外构建和功能验证后,研究者建立小鼠乳腺癌术后复发模型,以评估工程化乳腺类器官在体内局部治疗场景中的作用。该模型更接近术后残留病灶所处的局部环境,也能够检验类器官 depot 是否具备足够的体内滞留和递药能力。
实验分组包括未治疗、游离 DOX、DOX+ATRA、ATRA-DOX、未装药乳腺类器官、乳腺类器官与药物简单混合物,以及预装载 ATRA-DOX 的工程化乳腺类器官 eMO。研究团队通过生物发光成像、肿瘤体积监测和生存分析,比较不同处理方式对术后复发的影响。
结果为eMO 处理组的肿瘤复发信号降低,肿瘤体积增长受到抑制,并延长了小鼠生存时间。相较于“类器官+药物”简单混合处理,预装载前药的工程化类器官具有更强治疗效果,说明药物在泌乳样脂滴中的预先富集以及类器官介导释放,是该体系优于简单局部给药的重要因素。
经组织学检测,eMO 处理后肿瘤组织中凋亡相关信号增强,增殖相关信号降低,支持局部释放 DOX 对残留肿瘤细胞具有有效杀伤作用。研究还观察到肿瘤免疫微环境发生改变,提示该递药体系可能在直接化疗杀伤之外伴随免疫微环境重塑。
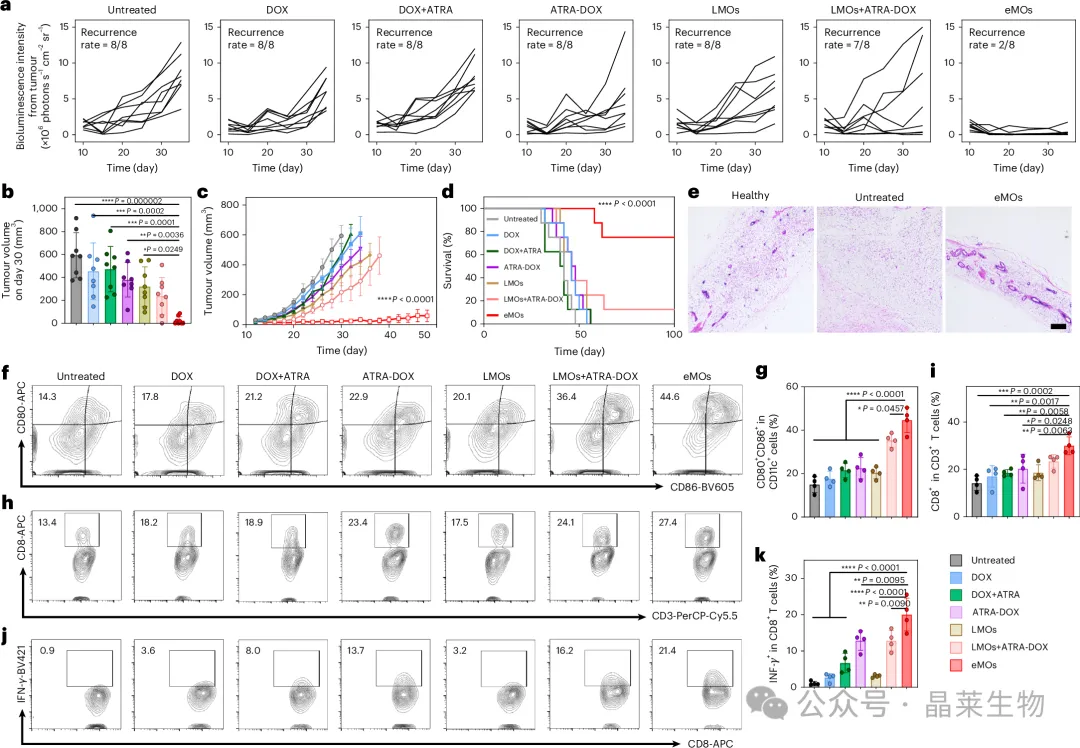
图3 | 工程化乳腺类器官在小鼠术后乳腺癌复发模型中的治疗效果 A. 术后复发模型建立与治疗流程;B. 不同处理组小鼠生物发光成像;C-D. 肿瘤复发信号及肿瘤体积变化;E. 各治疗组生存曲线;F-G. 肿瘤组织中细胞凋亡与增殖标志物检测;H. 工程化乳腺类器官局部递药抑制术后复发的机制示意。
4. 植入类器官参与乳腺组织重建并恢复泌乳功能
除局部递药外,该研究还评估了植入类器官与宿主乳腺组织的整合能力。与惰性缓释材料不同,乳腺类器官并不是单纯的载药支架。它含有乳腺上皮和肌上皮等细胞成分,植入后还可能参与乳腺导管样结构重建,因此需要同时评估其递药作用和再生能力。
体内实验显示,植入后的乳腺类器官能够在宿主组织内存留,并参与乳腺导管样结构形成。组织学结果显示类器官来源细胞与宿主乳腺组织发生结构整合,而不是单纯作为局部占位材料存在。
在妊娠和分娩相关模型中,接受类器官植入的小鼠出现泌乳功能恢复迹象。该结果表明,工程化乳腺类器官在术后局部递药之外,还可能作为再生种子参与腺体结构和功能重建。
结果显示类器官不再仅作为体外模拟组织发育或疾病状态的模型,而是被设计为能够在体内承担治疗、组织整合和功能修复任务的工程化细胞组织单元。
5. 人 iPSC 来源乳腺类器官验证平台转化潜力
为评估该策略在人源体系中的适用性,研究者构建了人 iPSC 来源乳腺类器官,并采用类似流程诱导其形成泌乳样表型、装载 ATRA-DOX,最终获得工程化人源乳腺类器官 eHMO。
人源乳腺类器官表现出乳腺相关分化特征,并具备前药装载和释放能力。在人源乳腺癌相关小鼠模型中,eHMO 能够抑制术后肿瘤复发,并促进人源乳腺组织样结构形成。
结果说明,工程化乳腺类器官 depot 的设计原则并不局限于小鼠来源细胞体系。理论上,若能够从患者自体细胞获得稳定、可控的乳腺类器官,再结合药物装载和局部植入,有可能形成兼具术后抗复发和组织再生功能的个体化治疗平台。
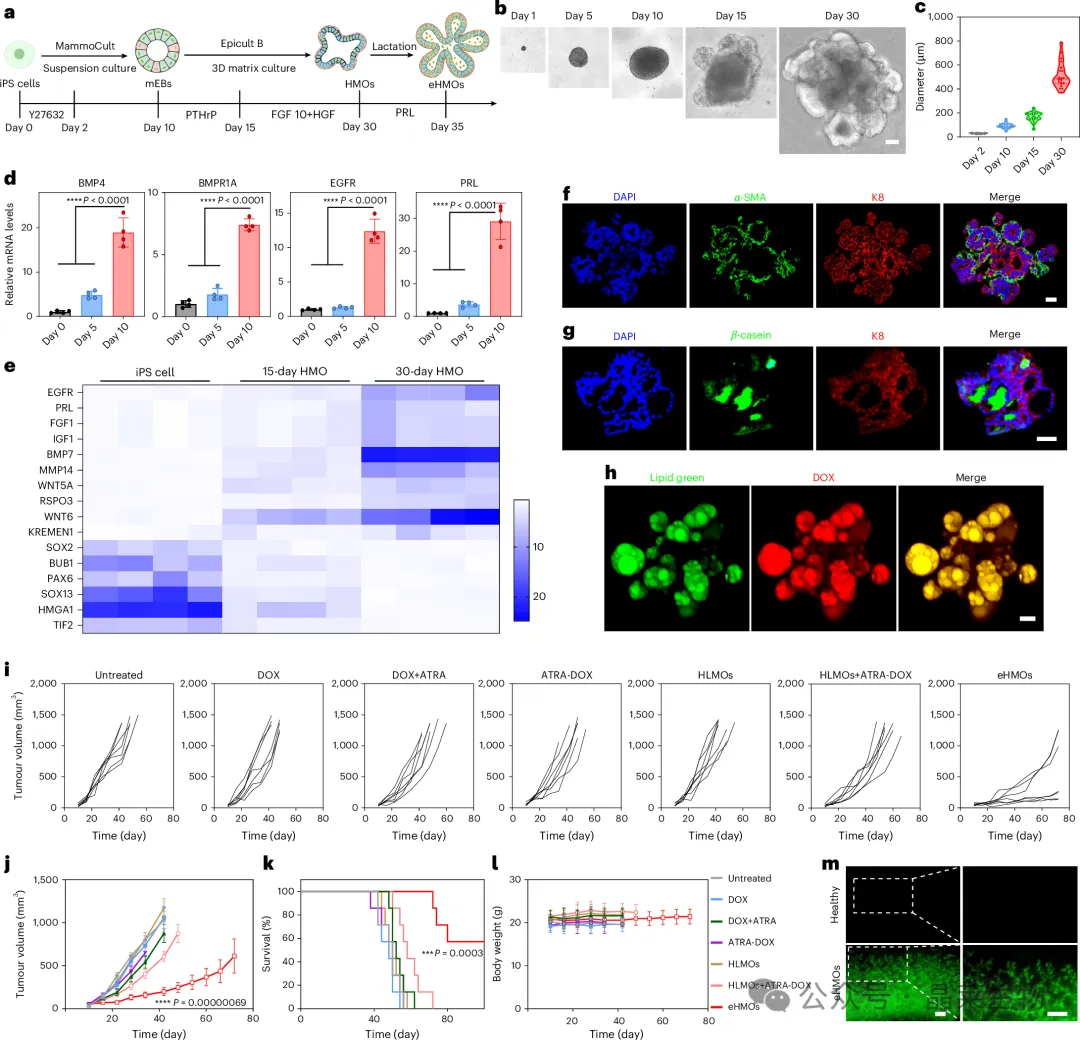
图4 | 人 iPSC 来源乳腺类器官的构建及体内功能验证 A. 人 iPSC 来源乳腺类器官分化流程;B. 人源乳腺类器官形态及乳腺相关标志物表达;C-D. eHMO 的前药装载与释放能力;E. 人源乳腺癌术后模型治疗流程;F-G. eHMO 对术后复发的抑制效果;H. 人源乳腺类器官参与组织再生的模式总结。
03 研究意义
乳腺癌术后需要同时考虑两件事:一是尽可能清除术区残留肿瘤细胞,降低复发风险;二是修复肿瘤切除后留下的组织缺损。
本研究的意义在于,把这两件事放到了同一个类器官系统中。研究者先让乳腺类器官进入类似泌乳的状态,使其产生脂滴,再将亲脂性前药装入脂滴中。植入术区后,类器官可以释放含药脂滴,在局部发挥化疗作用,用于抑制残留肿瘤细胞再生长。
同时,乳腺类器官并不是单纯的载药材料。它本身含有乳腺相关细胞,植入后能够与宿主乳腺组织整合,参与导管样结构重建。动物实验中,接受类器官植入的小鼠后续还观察到泌乳功能恢复,说明其作用不只停留在药物释放层面。
类器官过去更多用于体外建模和药物筛选,而本研究证明,经过工程化改造后,类器官也可以被设计成植入体内的治疗和修复单元。
该策略目前仍处于动物实验阶段,未来是否能够走向临床,还需要解决人源类器官稳定制备、长期安全性、免疫相容性、药物释放可控性以及异常增殖风险等问题。但总体来看,这项研究为乳腺癌术后抗复发和乳腺组织修复提供了一种新的实验思路。
关于晶莱生物类器官研究中心
晶莱生物类器官研究中心以高仿生人体器官与肿瘤类器官模型为战略核心,为药企、创新biotech、高校及医院提供最具临床预测性的体外+体内一体化研究系统,覆盖科研服务、CRO药效评价、精准医疗、工具赋能四大场景。依托北京+长沙双研发中心3000㎡高端实验平台,显著提升IND申报成功率、降低临床失败风险,同时助力基础医学研究产出高水平成果。
晶莱生物类器官研究中心,不只是模型,更是让中国创新药更快走向全球的临床前加速器。
关于晶莱















