【五分钟讲实验】Western Blot实验样本制备攻略
时间:2026-04-29 阅读:101
写在前面
做过Western Blot的人都有体会:实验失败了,十次有八次问题出在样本制备上。转膜没转好?抗体孵育有问题?很多时候,问题早在处理样本的那一刻就埋下了。
今天就专门聊WB实验最基础也最关键的一环——样本制备。从组织/细胞蛋白提取到定量、变性,每一步的细节都拆开来讲。
一旦样本制备环节出现问题,会直接导致多种严重后果:
1. 蛋白降解:目标蛋白被分解成碎片,出现条带消失、杂带增多等现象。
2. 蛋白提取不完全:待检测的目的蛋白无法被有效提取,导致检测不到。
3. 蛋白修饰丢失:磷酸化等关键翻译后修饰信息丢失,无法反映真实状态。
4. 蛋白定量不准确:上样量不一致,实验结果失去可比性。
1. 细胞样本
保存条件:不能马上裂解的话,细胞沉淀必须速冻后-80℃保存(液氮或干冰乙醇浴),能放1个月左右。
注意:别直接放-20℃或4℃过夜。冰晶会刺破细胞,蛋白稳定性掉得很快。
2. 组织样本
长期保存:
① -80℃冰箱:半年左右
② 液氮:一年以上
注意:别反复冻融,建议分装成一次用的量。
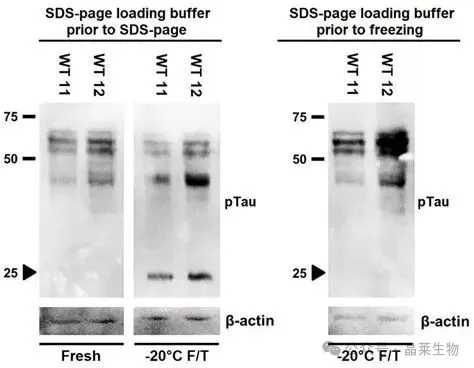
反复冻融导致 Tau 蛋白片段化的 WB 结果图
3. 其他样本类型
细菌/酵母:离心收菌体 → PBS洗2次 → 速冻保存(或直接裂解)。
植物组织:取样后液氮速冻,研磨时也得液氮保护,因为有细胞壁和酚类物质干扰。
血清/血浆:新鲜分离后直接-80℃保存,别反复冻融。
1. 裂解液的选择
裂解液分类及作用:
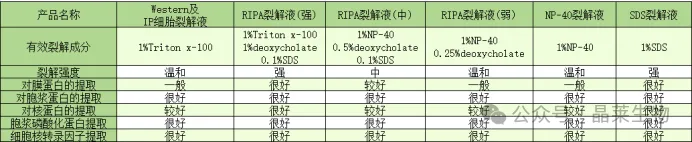
还原剂:DTT或β-巯基乙醇(可以裂解时加,也可以上样前加)。
蛋白酶抑制剂(必须加):常见的有PMSF(广谱丝氨酸蛋白酶抑制剂)、cocktail(复合抑制剂等)。
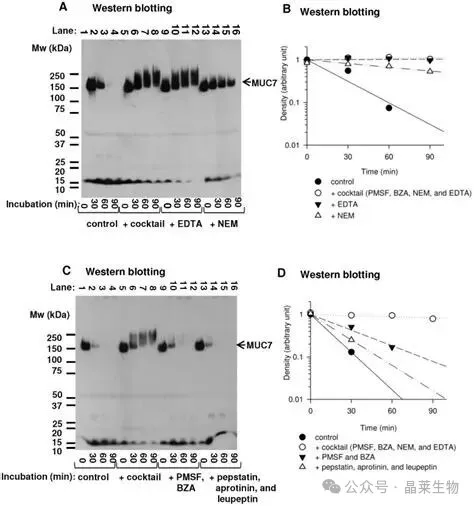
蛋白酶抑制剂对 MUC7 降解影响的 WB 结果图
磷酸酶抑制剂:检测磷酸化蛋白时必须加,比如NaF、Na₃VO₄等。
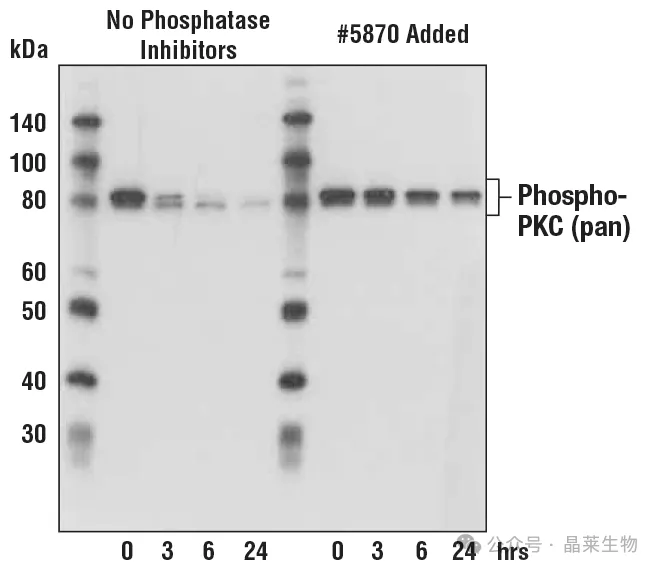
Phosphatase Inhibitor Cocktail / 磷酸酶抑制剂图
2. 细胞样本裂解步骤
① 悬浮细胞:
收集细胞沉淀(大概5×10⁶个细胞)按每10⁷细胞加100-200μL裂解液枪头吹打混匀,冰上放15-30min,每5-10min涡旋震荡10秒 4℃ 12000g离心 15-20min,吸上清(这就是总蛋白)到新离心管,沉淀扔掉。
② 贴壁细胞(拿6孔板说):
吸掉培养基,预冷PBS洗2次,吸干每孔加50-100μL裂解液,冰上放5min用细胞刮把细胞刮下来(朝一个方向刮,别弄出气泡),收集到离心管冰上继续裂解15min,中间震荡几次离心取上清。
③小经验:
裂解液用量要合适:太少提取不充分,太多蛋白浓度太低要是蛋白吹打后仍有沉淀或浓度低,可以超声处理(超声破碎仪,冰浴中超声3-5次,每次3-5秒,间隔30秒),能有效破碎细胞和DNA,提高产量、浓度。

3. 组织样本裂解步骤
方法一:液氮研磨(最经典)
组织块从-80℃拿出来,放预冷研钵里(研钵提前用液氮预冷)倒入液氮,用研杵把组织敲碎,磨成细粉(过程中不断加液氮保持低温)粉末转到预冷离心管,加适量裂解液(大概每50mg组织加500μL)涡旋混匀,冰上裂解30min,每10min震荡一次4℃ 12000g离心15min,取上清。
方法二:机械匀浆(研磨效果好)
组织块剪碎后放离心管,加预冷裂解液,用电动机器提前预冷(或手持组织研磨器在冰上匀浆),每次10-15秒,重复3-4次,到看不见明显组织块冰上继续裂解15-30min离心取上清。
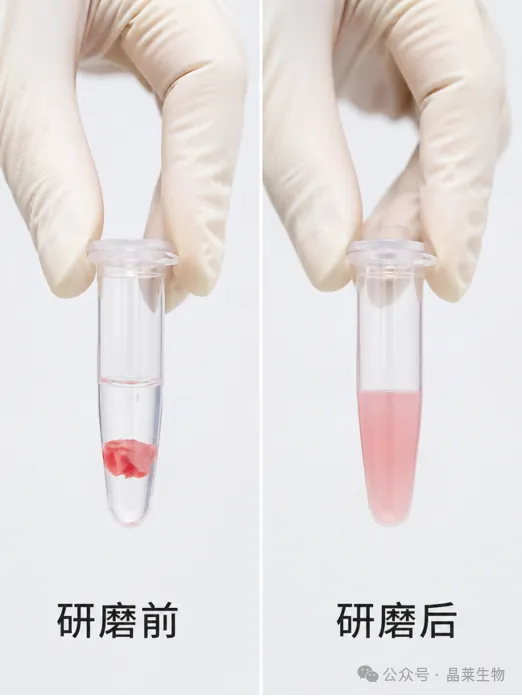
注意:整个过程必须低温(冰上或4℃),防止蛋白酶活跃对于骨、肌肉这些韧性组织可以用钢珠震荡研磨仪脂肪组织裂解后上清上层会有油,得小心吸下层清液。
裂解后的蛋白样品必须定量,才能保证每孔上样量一致,结果才有可比性。
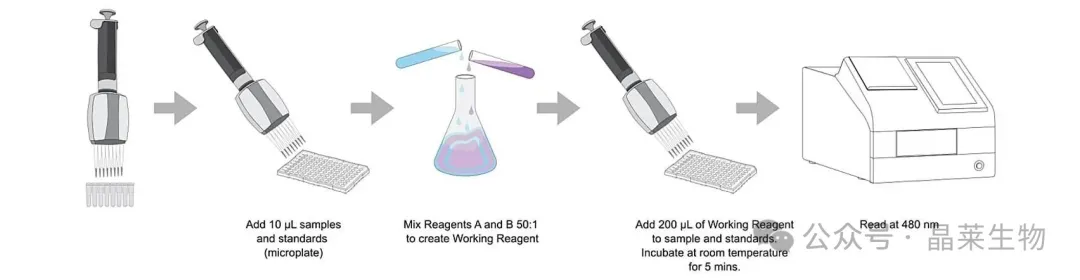
常用方法:BCA法
原理:蛋白在碱性条件下把Cu²⁺还原成Cu⁺,BCA和Cu⁺结合形成紫色复合物,562nm吸光度和蛋白浓度成正比。
步骤:配BCA工作液(A液:B液=50:1)BSA标准品按梯度稀释,各浓度标准品和待测样品(可以稀释不同倍数)加到96孔板,每孔加200μL工作液,37℃孵育30min 酶标仪测 562nm 吸光度根据标准曲线算样品浓度。
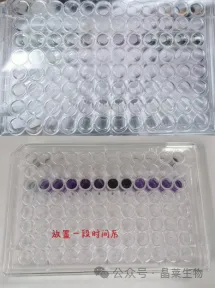
注意:样品中若有高浓度还原剂(比如DTT)或螯合剂(EDTA),会干扰BCA法,可以用Bradford法(考马斯亮蓝法)代替样品最好做2-3个稀释度,取在标准曲线中间段的浓度定量后,所有样品用裂解液调到相同浓度。
目的:让蛋白和SDS充分结合,形成带负电荷的棒状结构,消除电荷和形状对电泳迁移率的影响。
步骤:取一定体积的蛋白样品加5×或6×上样缓冲液(含SDS、溴酚蓝、甘油、还原剂如DTT或β-巯基乙醇),稀释成1×混匀。
煮沸:100℃加热5-10min(金属浴或沸水浴)马上冰上冷却,短暂离心后就可以上样或-20℃保存。

注意:还原剂最好现加(DTT容易氧化失效)煮沸时间别太长,不然蛋白可能聚集或脱氨膜蛋白这些难溶蛋白,可以适当延长煮沸时间(但别超过15min)煮沸后样品要是出现沉淀,说明蛋白可能聚集了或者变性不充分。
问题1:蛋白降解(条带变弱、出现杂带)
可能原因:样本处理时间太长,没低温操作没加蛋白酶抑制剂或抑制剂失效反复冻融。
解决办法:全程冰上操作,所有试剂预冷裂解液必须临用前加新鲜PMSF(PMSF在水里半衰期短,得现加现用)用蛋白酶抑制剂cocktail(广谱),样品分装保存,别反复冻融。
问题2:蛋白浓度太低
可能原因:细胞/组织量不够、裂解液体积太大、裂解不充分、蛋白降解了。
解决办法:增加起始样本量、适当减少裂解液用量、裂解后超声处理(注意冰浴)、延长裂解时间(但别超过1小时)等方法浓缩蛋白。
问题3:磷酸化蛋白检测不到
可能原因:磷酸酶抑制剂没加或失效样本处理过程中磷酸化被去掉。
解决办法:裂解液必须加磷酸酶抑制剂(比如NaF、Na₃VO₄)全程冰上操作,动作快组织样本离体后马上速冻,防止去磷酸化。
问题4:煮沸后出现絮状沉淀
可能原因:蛋白浓度太高,煮沸时聚集、还原剂不够、样品里有高浓度去垢剂。
解决办法:降低样品浓度、增加上样缓冲液里还原剂的比例、适当稀释样品或换裂解液。
1. 宁可多洗两遍PBS,也别省:残留的培养基、血清会干扰裂解和电泳。
2. 蛋白酶抑制剂别省:就算做普通内参检测,不加PMSF也可能降解。
3. 磷酸化蛋白检测要全程冰上操作:如果不低温操作,磷酸酶会在几秒钟内迅速把刚磷酸化的蛋白去磷酸化。
4. 裂解液体积宁少勿多:浓度高可以稀释,浓度太低就很难补救了。
5. 超声处理:细胞裂解不彻底、DNA粘稠的情况,超声几秒效果明显(注意功率别太大,防止蛋白断裂)。
6. 蛋白定量一定要做:凭感觉上样是新手最容易踩的坑。
7. 煮沸时间别太长:5分钟够了,太长反而可能让蛋白聚集或降解。
8. 样品制备完尽快用:-80℃保存的样品,也最好3个月内用掉,放久了可能降解。
结语
WB结果稳不稳,很多时候从样本制备这一步就决定了。
从采样保存、裂解提取,到蛋白定量、变性上样,每一步看起来都很基础,但只要低温没做好、抑制剂没加、反复冻融了,或者上样量不一致,后面的条带就很容易“看不懂”。
所以不如从制样环节就把关键点做扎实:全程低温、及时裂解、合理控制裂解液体积、做好蛋白定量、避免过度煮沸和反复冻融。
这些细节做到位,WB结果的稳定性通常会好很多。
关于晶莱















