【顶刊学习IF=113.3】脑类器官研究核心技术路线与研究思路启发!
时间:2026-04-29 阅读:101

脑类器官的核心价值:
①人源多能干细胞(iPSC/ESC)自组装形成3D人脑结构,可模拟胚胎-胎儿期皮层发育。
②能做进化、发育疾病、感染、药物筛选四大方向研究,是目前最接近人脑的体外模型。
③可实现患者特异性建模、基因编辑、高通量筛选。
脑类器官=体外迷你人脑+可操控、可重复、可高通量的神经发育与疾病研究平台。
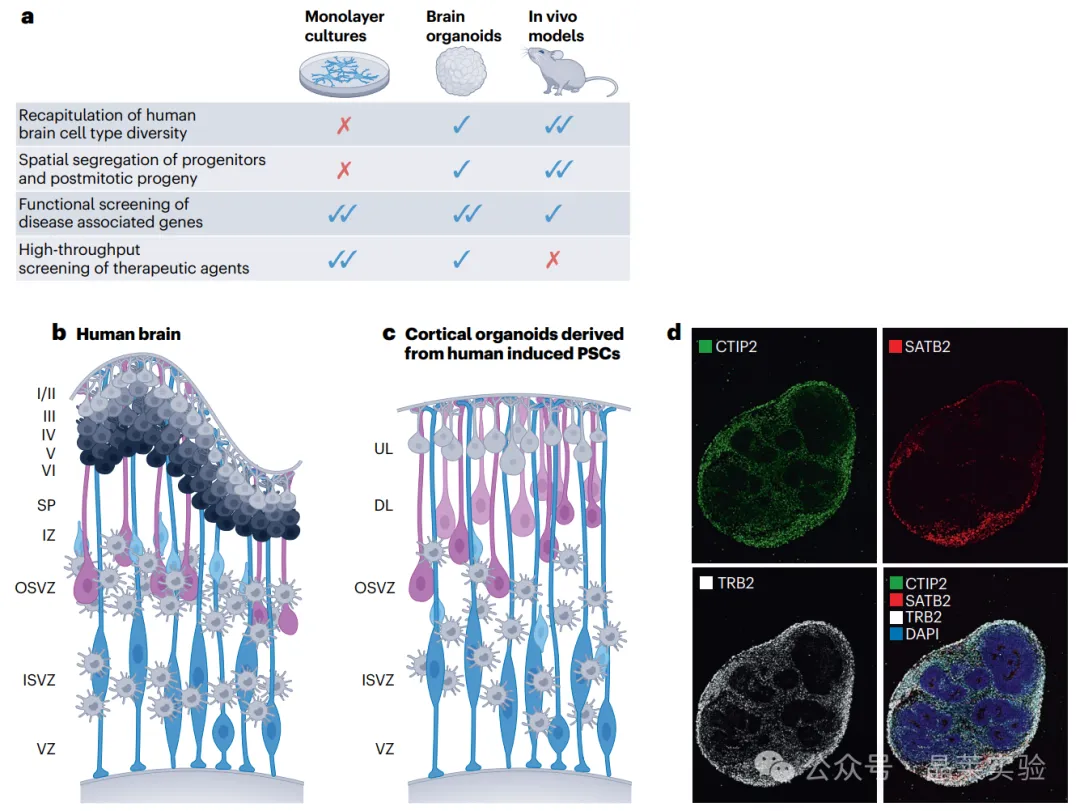
a.对不同模型系统复刻人脑细胞类型多样性、祖细胞与有丝分裂后子代的空间分离、疾病相关基因的功能筛选、治疗药物的高通量筛选能力进行评估。评分标准中,叉号代表该特征的复刻程度极低,单对勾代表中等复刻程度,双对勾代表高复刻程度。
b.人脑的分层结构,包括脑室区(VZ)、中间区(IZ)、内侧脑室下区(ISVZ)、外侧脑室下区(OSVZ)、亚板(SP)与皮层的6个分层(I-VI层)。
c.人诱导多能干细胞来源的皮层类器官中,皮层细胞类型以假分层结构有序排列。
d.2月龄人多能干细胞来源皮层类器官中,皮层命运的祖细胞通过TBR2标记,深层神经元(CTIP2)与浅层神经元(SATB2)可视化成像,显示出这些细胞类型的假分层结构。
1.非引导式(Minimallyguided)
不加外源形态发生素,靠细胞自组装,一个类器官里能长出多个脑区(皮层、海马、中脑等)。
优点:高度模拟体内自组织;缺点:批次差异大,不均一。
2.引导式(Guided)
用双SMAD抑制+WNT抑制定向诱导成单一脑区(如皮层、丘脑、中脑)。
优点:重复性高、细胞成分均一,适合疾病建模与筛选;缺点:人工干预强。
建议:优先做引导式皮层类器官,最稳定、发文最成熟。
3.模型制备核心
①拟胚体(EB)形成→神经诱导→基质胶(Matrigel)包埋→振荡培养→长期成熟培养
②关键控制点:细胞接种密度、ROCK抑制剂使用、培养基更换节奏、氧浓度。
③常见问题:坏死、腔室不形成、分化不纯→根源多在EB质量与神经诱导时机。
4.受体内脑发育启发的脑类器官制备方案示意图
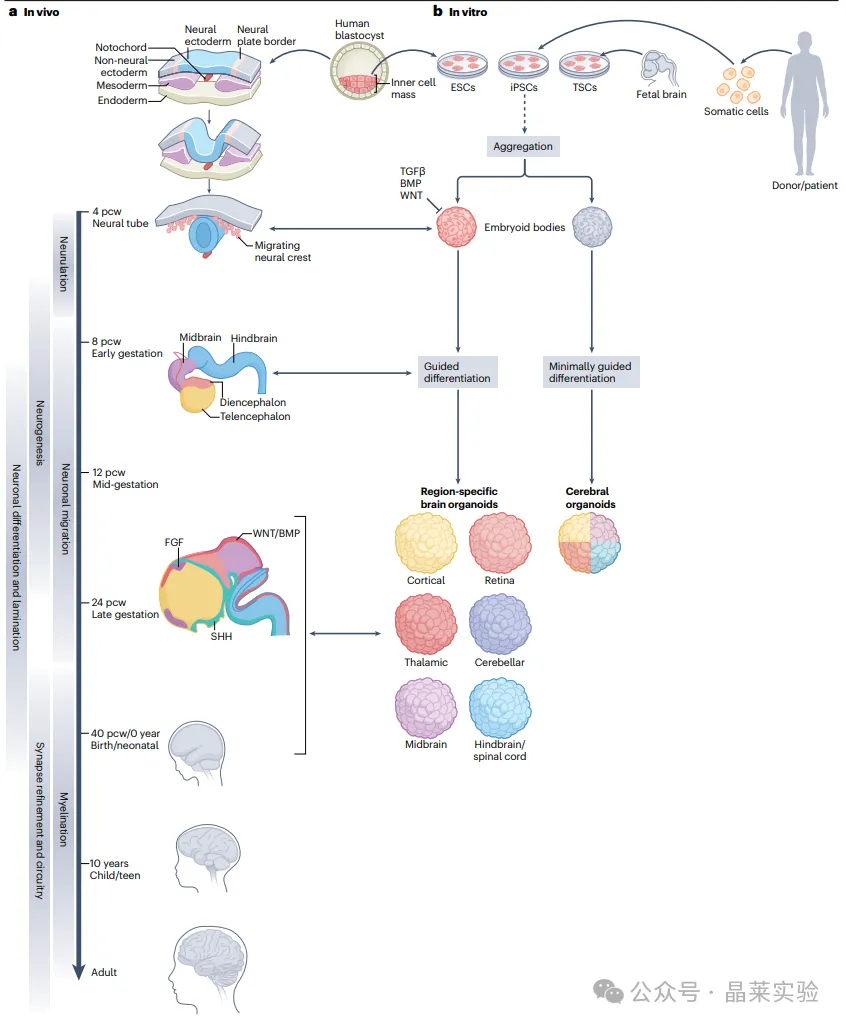
a.人神经系统发育的关键阶段与过程。外胚层形成神经板(神经诱导)后,神经板折叠形成神经管,随后神经管分化为前脑、中脑与后脑(神经胚形成与区域化)。随着神经元(神经发生)与神经胶质细胞(胶质发生)的生成,细胞发生成熟过程,形成细胞构筑结构(神经元迁移),并进一步成熟(轴突导向、突触发生、髓鞘形成与突触修剪),最终实现神经系统的正常发育。在该过程中,关键形态发生素相互作用并形成梯度,建立复杂的基因表达模式,在整个神经系统发育过程中,引导细胞命运决定与形态发生。
b.胚胎干细胞(ESCs)、诱导多能干细胞(iPSCs)或人胎儿组织干细胞(TSCs),首先被组装为三维球体或拟胚体,其可自组装形成神经外胚层结构。
非引导性方案中,多能干细胞聚集为拟胚体,不添加用于诱导特定脑区身份的生长因子,最终形成的类器官包含不同脑区身份的组织。
引导性方案旨在生成特定的区域身份,提升细胞类型的一致性。该类方案通常会抑制SMAD通路,最常使用双SMAD抑制策略,通过小分子抑制剂靶向TGFβI型受体与BMPs;同时在类器官制备的早期阶段抑制WNT信号。
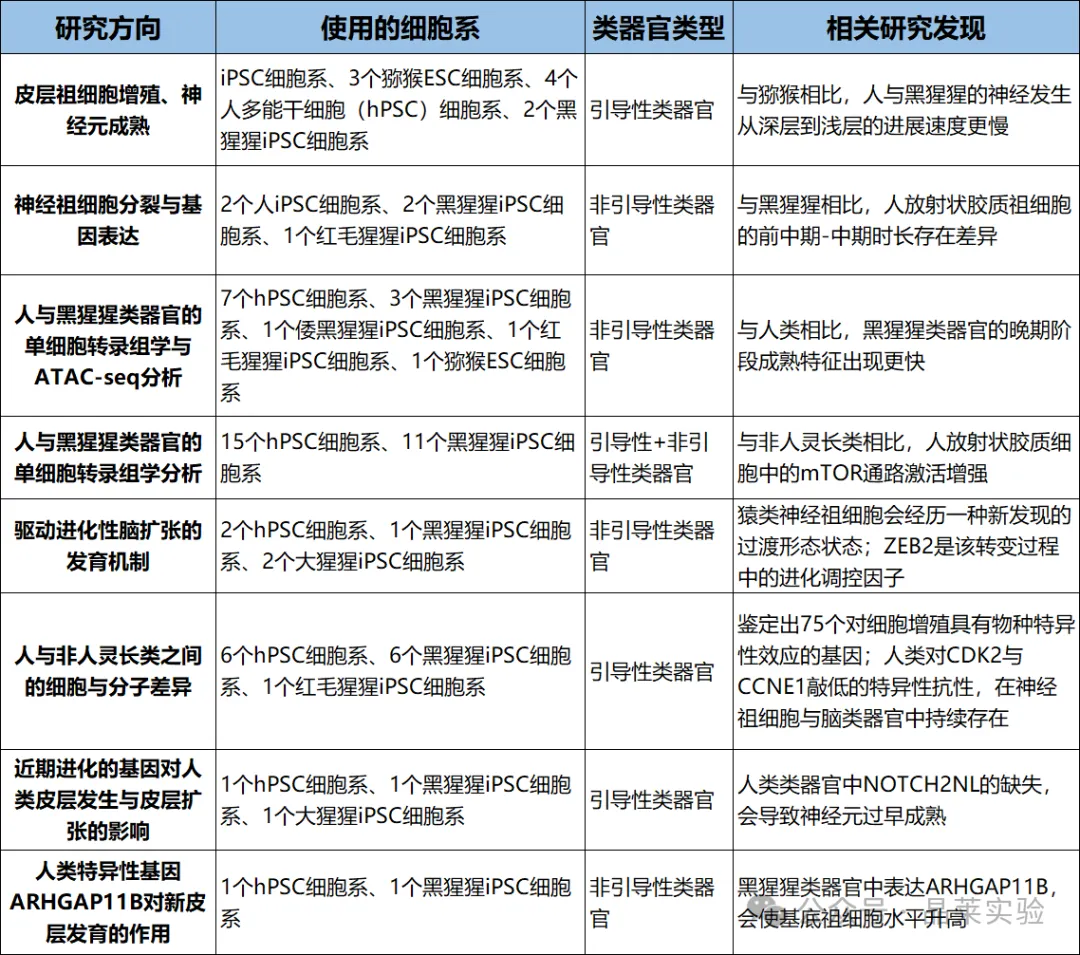
方向1:灵长类脑进化研究(基础生物学顶刊最爱)
核心问题:人脑为什么更大、更复杂?
研究路径:人vs黑猩猩/大猩猩/猕猴→类器官对比→找细胞行为差异
(神经发生速度、细胞周期、祖细胞形态、基因表达);
关键基因:ARHGAP11B、NOTCH2NL、ZEB2、HARs;
结论:人类神经上皮细胞形态转变更慢→祖细胞池更大→神经元更多。
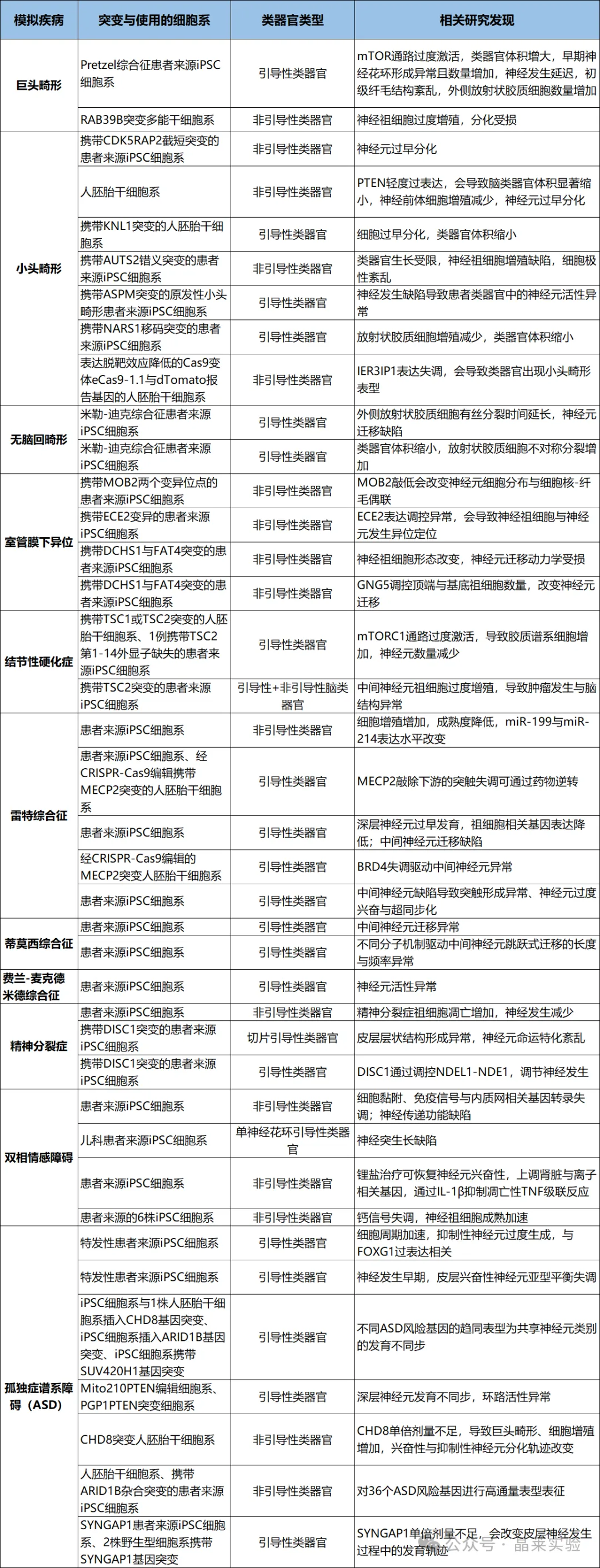
方向2:神经发育与精神疾病建模覆盖几乎所有热门疾病:
皮层畸形:小头畸形、巨头畸形、无脑回、室管膜下异位;
神经发育病:Rett综合征、脆性X、天使综合征、Timothy综合征
孤独症(ASD)、精神分裂症、双相情感障碍。
研究路径:患者iPSC→类器官→表型(增殖/迁移/成熟/电生理)→机制→药物筛选。
利用皮层类器官模拟人脑疾病的研究示例
方向3:神经系统感染疾病研究(速度快、易出结果)
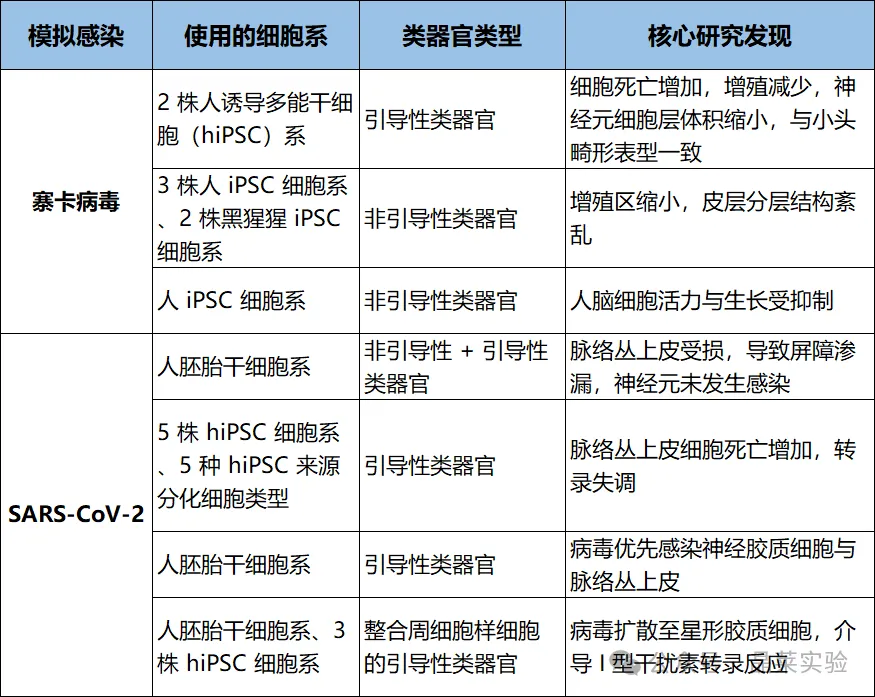
经典模型:寨卡病毒、新冠病毒、CMV、HSV-1、HIV、朊病毒;
已有的相关研究发现:病毒优先感染神经祖细胞、脉络丛、胶质细胞→导致小头畸形/发育异常;
应用:快速筛选抗病毒药物、验证保护机制。
利用皮层类器官模拟脑部感染性疾病的里程碑及最新研究
提升当前人脑类器官培养的生理相关性,无偏倚解析细胞复杂性
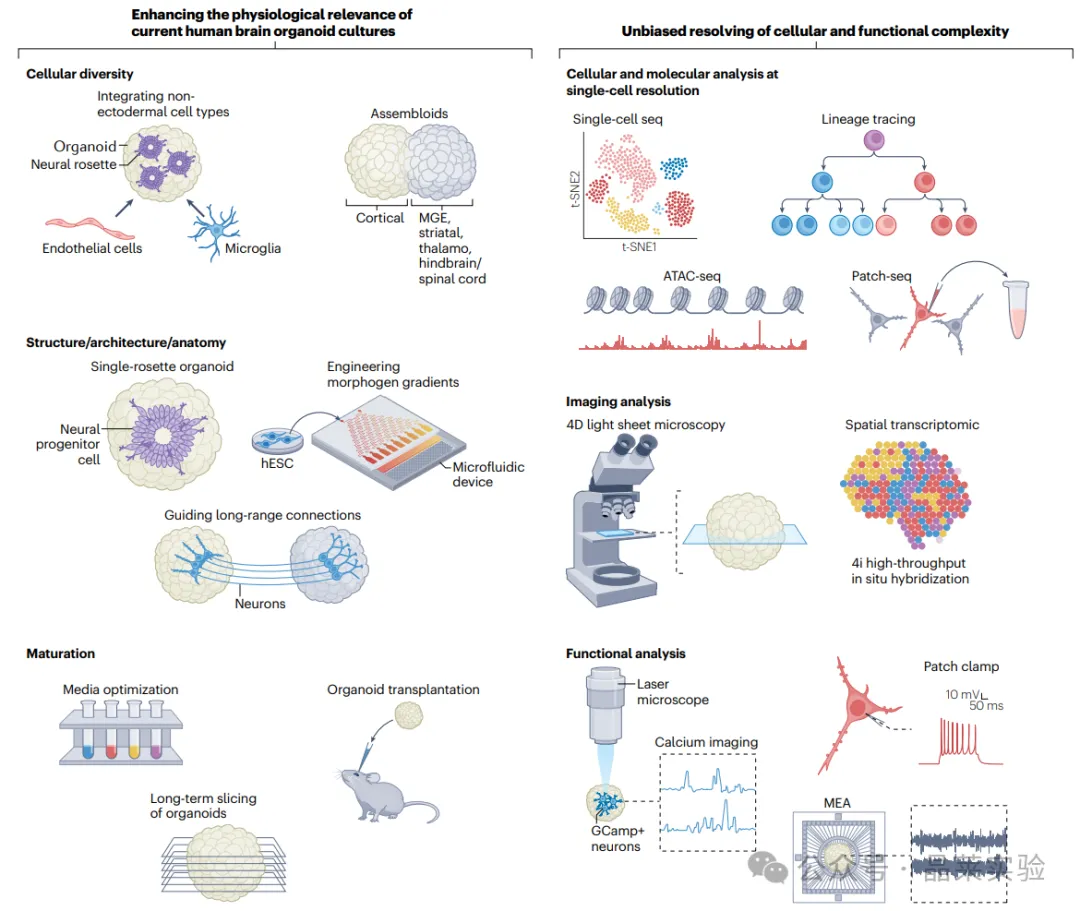
左图:多学科技术整合,用于优化脑类器官的制备;右图:类器官的表征技术。
①细胞多样性提升:整合内皮细胞、小胶质细胞等非外胚层细胞类型,可增强类器官的细胞多样性;融合皮层、内侧神经节隆起(MGE)、纹状体、丘脑、后脑/脊髓等多个区域特异性类器官,可构建被称为组装类器官的培养体系,实现不同脑区或器官系统的对比研究。
②结构/解剖/细胞构筑优化:采用单神经花环类器官制备方案、工程化形态发生素递送,以及微流控系统培养,可引导不同区域特异性类器官之间的长距离连接形成,从而改善脑类器官的结构、解剖与细胞构筑。
③成熟度提升:通过优化培养基成分、脑类器官移植,或对长期培养的类器官进行切片培养,可提升类器官的成熟度。
④单细胞水平的细胞与分子分析:ATAC-seq、单细胞RNA测序、Patch-seq与谱系示踪技术,可对类器官的细胞与分子谱进行表征。
⑤成像分析:迭代间接免疫荧光成像(4i)、4D光片显微镜与空间转录组学等成像技术,可提供类器官中不同细胞类型的空间信息;谱系示踪技术可同时提供空间信息与谱系树轨迹。
⑥功能分析:膜片钳、钙成像与多电极阵列(MEA)技术,可用于脑类器官成熟度的功能评估。
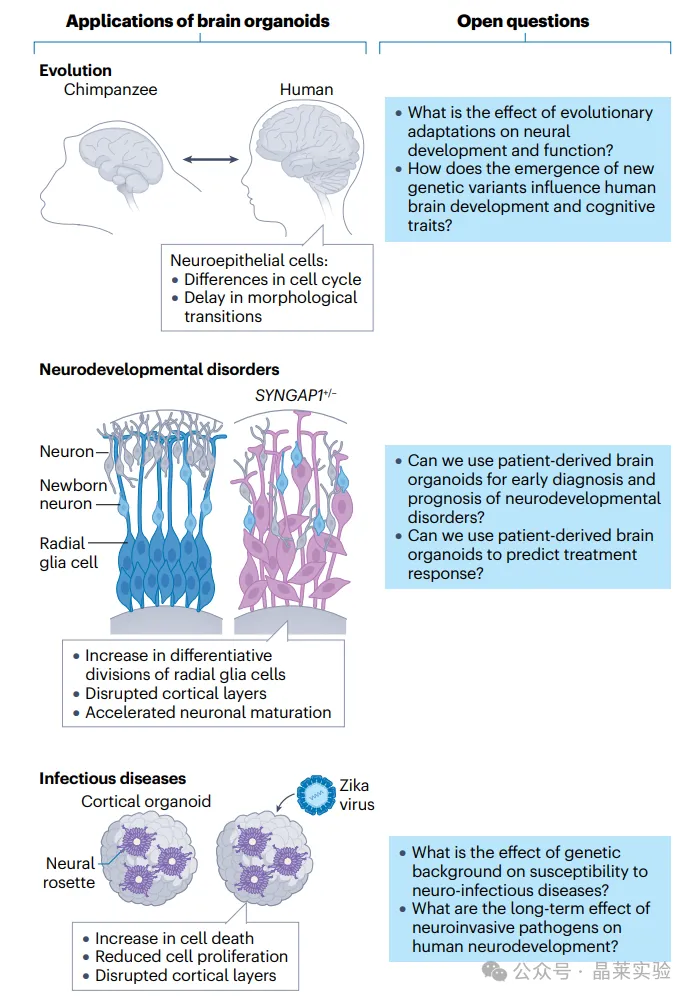
脑类器官已被证实,可深化我们对进化、神经发育障碍与感染性疾病的理解,有望解决动物模型无法回答的科学问题。图中展示了部分关键研究发现,这些发现为人类大脑扩张的潜在机制(上)、神经元分化及相关疾病(中)、寨卡病毒感染的影响(下)提供了全新见解。
未来的优化方向,可能还将聚焦于通过多种生物工程方法,提升神经元成熟度、连接性,以及不同区域身份类器官之间功能性环路的形成。构建可模拟不同脑区类器官间宏观环路的平台,还能够混合搭配不同遗传背景的类器官,从而揭示体内研究难以解析的、不同脑区的选择性易损性。
关于晶莱














